*仅供医学专业人士阅读参考
梁斐教授揭示IMpower133研究设计背后的奥秘。
近年来,随着免疫治疗的发展,广泛期小细胞肺癌(ES-SCLC)治疗的困境逐步改变。IMpower133是ES-SCLC领域里程碑式的研究,研究中阿替利珠单抗联合卡铂和依托泊苷(EC)一线治疗ES-SCLC取得了总生存期(OS)和无进展生存期(PFS)的双重获益。据此,阿替利珠单抗联合化疗在美国、中国等多个国家相继获批ES-SCLC一线治疗适应证,使SCLC正式进入免疫治疗时代。与此同时,随着CASPIAN等研究数据的公布,ES-SCLC免疫治疗迎来更多突破。
对此,“医学界”特邀复旦大学附属中山医院梁斐教授,从统计学视角来解读IMpower133研究在研究设计、结果等方面的特点,分享不同研究结果间接比较的注意事项,为临床ES-SCLC一线治疗优化选择提供参考。
IMpower133研究回顾:首次ES-SCLC一线免疫治疗获得PFS和OS双终点阳性
IMpower133是一项全球、双盲、安慰剂对照的III期研究。研究纳入403例未经治疗的ES-SCLC患者,按1:1随机分配接受4个周期阿替利珠单抗+化疗或安慰剂+化疗诱导治疗,之后继续使用阿替利珠单抗或安慰剂维持治疗,直到出现不可耐受的毒性、疾病进展或没有临床获益。
值得一提的是,与其他SCLC免疫治疗研究不同的是,该研究采用了PFS、OS双终点设计。

图1. IMpower133研究设计
梁斐教授指出,虽然OS是临床研究的金标准,是临床医生和患者最关注的终点,也是药监机构非常认可的终点。但实际上PFS也具有非常重要的临床意义,能够评价治疗方案能否延缓肿瘤进展、提高患者生活质量。
IMpower133研究采用OS和PFS双终点的设计,在统计学上的要求更高。其中两个关键要求是:在不同研究终点之间合理分配α值;针对每个研究终点计算样本量,确保有足够的统计学效能来下确证性结论。
对于III期临床研究,特别是确证性的注册关键研究,整体α值只有0.05。如果采用双终点的话,则意味着每个终点初始分配的α值会更小,因此每个终点成功的难度相比单终点更大。也正因如此,双终点如果能够同时达到,那么其临床意义可能会更加重要。
而且,从统计学角度来讲,只有参与了α值分配并计算样本量的研究终点,才能够给出确证性结论,用来支持适应证获批,没有参与α控制的研究终点不能用于支持药品说明书声称的获益。
IMpower133研究的双终点设计符合上述要求,研究将整体的0.05的α在OS和PFS之间进行了分割,OS和PFS初始分别分得0.045和0.005,并且采用了α回收策略。同时从样本量方面考虑,针对OS和PFS终点,IMpower-133研究都有足够的统计学效能下确证性的结论。在这样情况下得到的PFS结果的阳性结论无疑是更加可信的。
凭借阿替利珠单抗的出色疗效,最终IMpower133研究不负众望,两个终点均得到都满足了统计学的要求,达到了预设的终点,且均为最高等级证据。
2018年《新英格兰医学杂志》发表了IMpower133研究结果显示,中位随访13.9个月时,阿替利珠单抗组和安慰机组的中位OS分别为12.3个月和10.3个月(HR=0.70,95%CI:0.54-0.91;P=0.007),中位PFS分别为5.2个月和4.3个月(HR=0.77;95%CI:0.62-0.96;P=0.02)[1]。由于疗效非常好,OS和PFS在中期分析时已经达到了阳性结果,IMpower133研究提前终止。
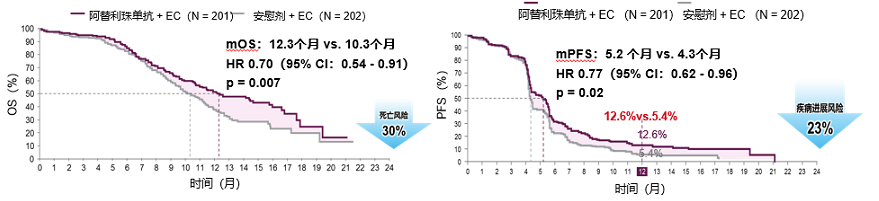
图2. IMpower133研究主要终点OS和PFS结果
IMpower133研究是SCLC领域免疫治疗第一个成功的全球多中心的研究,也是目前唯一OS和PFS双终点成功的临床研究,为后续临床研究立下了标杆。
不同治疗方案如何选择?结果的稳定性和可信度是重要考量因素
ES-SCLC一线治疗目前已有多项研究结果公布,然而由于缺乏头对头直接比较,因此无法对不同药物的疗效高低做明确判定。
梁斐教授指出,在这种情况下,临床医生在进行治疗选择时,需要借助一些指标来进行探索性判定,包括中位值、HR值及OS率等。其中HR值反映的是两条生存曲线全程的差异,因此比较全面和稳定。HR值是临床研究关注的重点,也是欧洲肿瘤内科学会(ESMO)和美国临床肿瘤学会(ASCO)临床获益评价量表中评估药物获益的一个重要指标。
中位值的提高程度和OS率则是临床医生更加容易理解的指标,但值得注意的是,研究报告中的中位值和OS率通常都是估计的结果,具有一定的不稳定性。如果随访时间不够,或者研究数据成熟度较低,此时也可以估计出中位值以及1年或2年的OS率。但若存在以下情况,如中位随访时间短于中位值,95%置信区间较宽,或者截至中位随访时间的风险人数(No. at risk)远远少于试验组总人数的一半,则意味着中位值可能不够稳健。随着随访时间的延长,中位值及OS率可能发生变化,甚至在某些情况下发生明显的变化。
因此,临床医生在解读中位值和OS率时,还应关注其置信区间、数据的成熟度以及中位随访时间,根据结果的稳定性和可信度进行综合判断。比如IMpower133研究中,阿替利珠单抗组的中位OS为12.3个月,中位随访时间已经达到了13.6个月,因此中位OS结果非常稳定。
SCLC免疫治疗研究未来探索方向展望
虽然免疫治疗已经改变了整个SCLC一线治疗的模式,但是与非小细胞肺癌相比,SCLC患者的整体预后仍相对较差。
梁斐教授表示,当前SCLC免疫治疗最大的问题就是,如何在免疫联合化疗的基础上进一步提高疗效。未来,临床上应探索免疫+化疗+其他药物、免疫+化疗+放疗等更多联合治疗模式,免疫治疗跨线能否进一步延长OS,以及探寻合适的疗效预测生物标志物以筛选出免疫治疗优势人群。
为了解决这些问题,除了开展临床试验外,临床医生还可以通过开展真实世界研究,对临床实践中对不同的治疗方案及生物标志物进行初步探索和分析。如果提示有获益,则可以进一步开展单臂研究、小样本随机对照临床研究,并在此基础上通过多中心的大型III期临床研究来得出明确结论。
未来期待更多像IMpower133研究这样高级别的循证医学证据出炉,让更多的SCLC患者免疫治疗中获益。
专家简介

梁斐 教授
复旦附属中山医院,生物统计室,统计师
复旦大学循证医学中心成员
上海抗癌协会癌症预防与筛查委员会委员
CSCO青年委员会统计小组成员
以第一作者(含共一)或通讯作者在JCO, Annals of Oncology, JNCI, European Journal of Cancer 等杂志发表SCI论著15篇,累计影响因子超过150
以第一作者在NEJM, Lancet, Lancet Oncology, JCO 发表Letter 8篇
JNCI, Clinical Cancer Research, Theranostics审稿人
作为统计师参与数十项研究者发起的临床研究,相关成果发表于JCO, Annals of Surgery等杂志
主要研究方向:临床试验设计及统计,临床研究方法学
参考文献:
[1]Horn L, Mansfield AS, Szczęsna A, et al. First-Line Atezolizumab plus Chemotherapy in Extensive-Stage Small-Cell Lung Cancer. N Engl J Med. 2018 Dec 6;379(23):2220-2229.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |