*仅供医学专业人士阅读参考
2022 WCLC有哪些重磅研究精彩亮相?
国际肺癌研究协会(IASLC)世界肺癌大会(WCLC)作为世界上最大的肺癌和其他胸部恶性肿瘤学术会议,每年都受到全球专业人士的广泛关注。小编梳理了2022年WCLC大会上与KRAS突变非小细胞肺癌(NSCLC)靶向治疗相关研究进展[1-4],供学习参考。
Sotorasib联合SHP2抑制剂在KRAS p.G12C突变NSCLC和其他实体肿瘤中的应用
(摘要号:OA03.03)
Sotorasib是一种特异的、不可逆的KRAS G12C抑制剂。在CodeBreaK100 I/II期试验中,受体酪氨酸激酶 (RTK) 的基因组改变被认为是sotorasib耐药的常见机制。在动物实验中,sotorasib与SHP2抑制剂联合使用可损伤RAS的RTK信号传导,增强抗肿瘤疗效。
一项研究报告了sotorasib联合RMC-4630(一种小分子SHP2抑制剂)治疗KRAS p.G12C突变NSCLC和其他实体肿瘤的安全性和疗效数据。2022年WCLC大会公布了NSCLC患者的疗效结果,截至2022年4月11日,纳入11例 NSCLC 患者,既往治疗的中位线数为3,约一半患者(n=5;45%)接受过KRAS G12C抑制剂治疗。在11例NSCLC患者中,3例 (27%) 经证实达到部分缓解 (PR),客观缓解率(ORR)为27%,其中2例缓解在数据截止时仍在持续;7例达到疾病控制,DCR(疾病控制率)达到64%。在6例既往未接受过KRAS G12C抑制剂治疗的患者中,ORR为50%,DCR为100%。
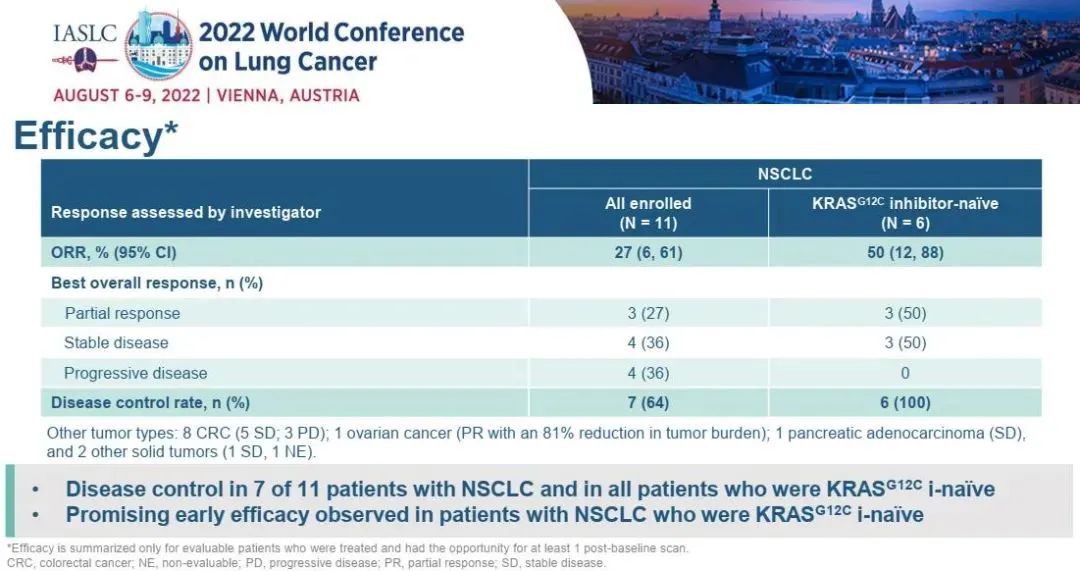
图1. sotorasib联合RMC-4630治疗NSCLC的疗效
在接受最高2个剂量RMC-4630联合sotorasib治疗的4例KRAS G12C抑制剂初治NSCLC患者中,3例 (75%) 达到经证实的PR,4例 (100%) 疾病控制。
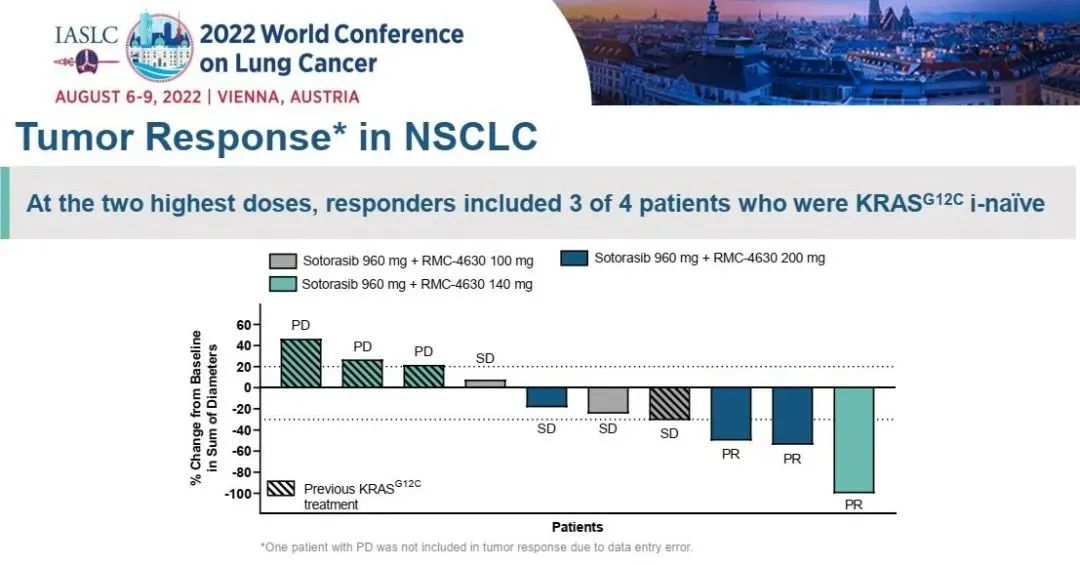
图2. NSCLC患者的肿瘤退缩
在安全性方面,sotorasib联合RMC-4630治疗是安全可耐受的。剂量递增完成时没有发生4级或以上的治疗相关不良反应(TRAE)。有63%的患者产生不同程度的TRAE,包括水肿、腹泻和口干。sotorasib联合RMC-4630在KRAS p.G12C突变的NSCLC患者中观察到了具有前景的临床活性,在未接受过 KRASG12C 抑制剂的患者中获益更为明显。
评估GDC-6036单药治疗KRAS G12C突变NSCLC患者的疗效
(摘要号:OA03.04)
GDC-6036是一种口服、高效、选择性KRAS G12C抑制剂,一项开放标签、剂量递增及剂量扩展研究,正在KRAS G12C突变的局部晚期或转移性实体瘤患者中进行GDC-6036单药或联合治疗,本次WCLC大会公布了GDC-6036单药治疗NSCLC的研究数据。
截至2022年5月13日,研究共入组135例患者,其中59例为NSCLC。在安全性方面,在NSCLC与其他实体瘤的治疗中,GDC-6036的常见TRAE为恶心、呕吐及腹泻,多为1级,7例患者发生的5级TRAE均与药物无关。总的来说,患者可通过支持治疗或剂量调整管理不良事件。在疗效方面,对于GDC-6036治疗的KRAS G12C突变NSCLC患者,未确认的ORR为53%(30/57),已确认的ORR为46%(26/57)。药代动力学分析表明,GDC-6036一天一次(QD)给药的半衰期与GDC-6036单次给药(50-400mg)一致,平均半衰期为13-17小时。剂量扩展中使用GDC-6036(400mg QD)治疗的患者预计可达到非临床研究中最大靶向共价结合的暴露量。

图3. KRAS G12C突变NSCLC患者的ORR
该研究证实,GDC-6036治疗实体瘤的耐受性良好,总体安全性可控。GDC-6036单药治疗既往接受过治疗的KRAS G12C 突变NSCLC显示出令人鼓舞的抗肿瘤活性。药代动力学支持GDC-6036一天一次的给药频率,并可在NSCLC中观察到高KRAS G12C靶点结合。
CodeBreaK 100/101研究: Sotorasib联合帕博利珠单抗或阿替利珠单抗治疗晚期KRAS p.G12C突变NSCLC
(摘要号:OA03.06)
2022年WCLC会议报道了sotorasib联合免疫治疗的首份研究结果。一项名为CodeBreaK 100/101的Ⅰb期研究,将既往未接受过KRAS G12C抑制剂治疗的KRAS G12C突变NSCLC患者分为12个队列,接受不同剂量的sotorasib联合帕博利珠单抗或阿替利珠单抗治疗。其中一半的队列为Lead-in,即患者在第一次联合用药前先进行21天或42天的sotorasib单药治疗。
研究纳入58例患者,中位随访12.8个月。在所有12个队列中,58例患者有17例患者达成确认缓解,ORR为29%,DCR为83%。在17例缓解患者中,中位缓解持续时间(DOR)为17.9个月。
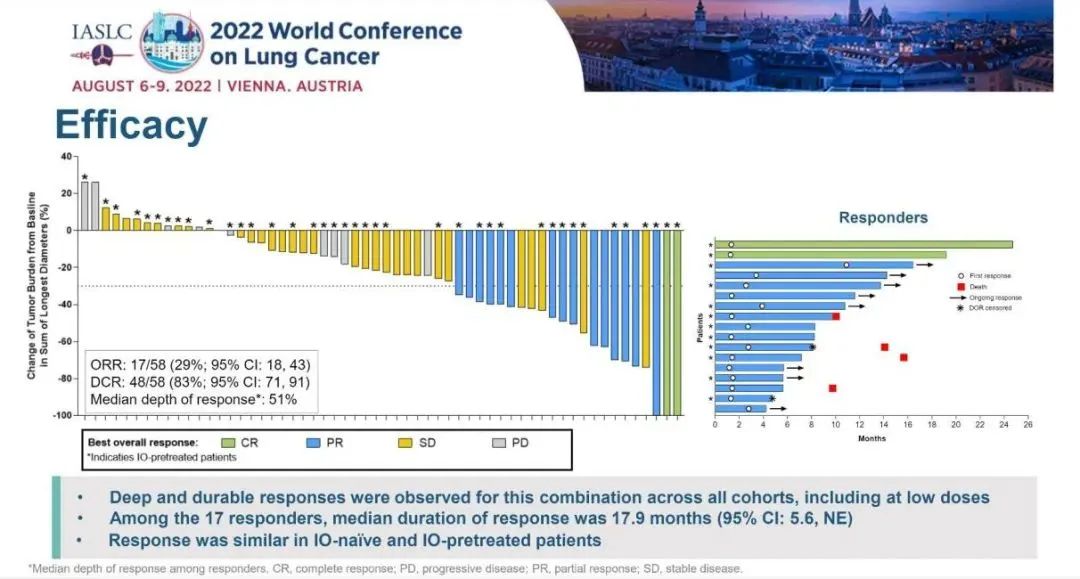
图4. Sotorasib联合帕博利珠单抗或阿替利珠单抗治疗的疗效
sotorasib联合免疫疗法的中位总生存期(OS)为15.7个月,在Lead-in队列和Concurrent队列,sotorasib联合帕博利珠单抗治疗的ORR分别为37%和32%,sotorasib联合阿替利珠单抗治疗的ORR均为20%,sotorasib联合帕博利珠单抗治疗获得了更有效的缓解。
在安全性方面,常见的3-4级TRAE发生率为59%,主要是肝毒性,表现为谷丙转氨酶(ALT)和谷草转氨酶(AST)水平升高。sotorasib组合免疫疗法发生3-4级TRAE的概率高于sotorasib单药疗法。与Concurrent队列相比,Lead-in队列表现出持久的临床疗效,3-4级TRAE的发生率较低。

图5. Sotorasib联合帕博利珠单抗或阿替利珠单抗治疗的安全性
一项Ⅰ期试验:D-1553在KRAS G12C突变NSCLC患者中的安全性和有效性
(摘要号:OA03.07)
D-1553是口服KRAS G12C的生物可利用抑制剂,可选择性地和不可逆地结合KRAS G12C突变蛋白,使其处于非活性GDP结合状态。一项Ⅰ期、开放标签、多中心研究针对接受标准治疗后进展的KRAS G12C突变的晚期或转移性NSCLC患者,进行D-1553的安全性、药代动力学(PK)和疗效评估。
截至2022年5月9日,研究共纳入79例NSCLC患者,患者接受过中位系统性治疗线数为2,其中42例患者(53.2%)既往接受了≥2线治疗。在2022年5月9日数据截止时,中位随访时间为21.7周。在所有79例患者中,53患者(67.1%)仍在接受治疗。68例患者(86.1%)发生TRAE,其中大部分为1-2级。最常见(≥20%)的TRAE是AST升高、ALT升高、γ-谷氨酰转移酶升高,结合胆红素升高和贫血。未报告5级TRAE。
其中所有剂量水平的73例患者可评估肿瘤反应:29例患者PR,38例患者疾病稳定(SD);ORR和DCR分别为39.7%(29/73)和91.8%(67/73),未达到中位DOR,但在29例有反应的患者中有25例患者(86.2%)仍在进行治疗中,其中14例患者的DOR≥12周。对于无进展生存期(PFS),57例(78.1%)受试者尚未达到事件。研究证实D-1553的耐受性良好,在经过大量预处理的KRAS G12C突变NSCLC中具有良好的抗肿瘤活性。
本材料由阿斯利康提供支持,仅供医疗专业人士参考
审批编号:CN-100805 过期日期:2023-8-15
参考文献:
[1] Bob T. Li, Kristen A Marrone, Christine M Bestvina, et al. Sotorasib in Combination with RMC-4630, a SHP2 Inhibitor, in KRAS p.G12C-Mutated NSCLC and Other Solid Tumors. 2022WCLC. OA03.03.
[2] Manish Patel, Wilson Miller, Jayesh Desai, et al. Phase I A Study to Evaluate GDC-6036 Monotherapy in Patients with Non-small Cell Lung Cancer (NSCLC) with KRAS G12C Mutation. 2022WCLC. OA03.04.
[3] Gerald Falchook, Greg Andrew Durm, Timothy F Burns, et al. CodeBreaK 100/101: First Report of Safety/Efficacy of Sotorasib in Combination with Pembrolizumab or Atezolizumab in Advanced KRAS p.G12C NSCLC. 2022WCLC. OA03.06.
[4] Hong Jian, Yiping Zhang, Zhengbo Song, et al. Safety and Efficacy of D-1553 in Patients with KRAS G12C Mutated Non-Small Cell Lung Cancer: A Phase 1 Trial. 2022WCLC. OA03.07.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |