*仅供医学专业人士阅读参考
快速get EGFR ex20ins 疾病负担与治疗进展
//
对于非小细胞肺癌(NSCLC)患者,EGFR常见突变位点ex19del和21外显子L858R突变目前已有多种靶向药物选择,但作为EGFR第三种常见突变位点的EGFR ex20ins曾经“久攻不破”。
为什么一定要“攻克”这个靶点?目前治疗进展如何?还有哪些未满足的需求值得进一步探索?
EGFR ex20ins是第三种常见的EGFR突变类型,且临床上这类患者可能比文献报告的数量更高。肺癌患者EGFR突变频率最高的是19号外显子缺失突变(Del19)和21号外显子L858R突变(被称为经典突变或常见突变),加起来占到全部EGFR突变的80%以上[1]。而EGFR ex20ins约占所有NSCLC腺癌突变的2%,所有EGFR突变的NSCLC病例的6%-10%[2-11](图2)。
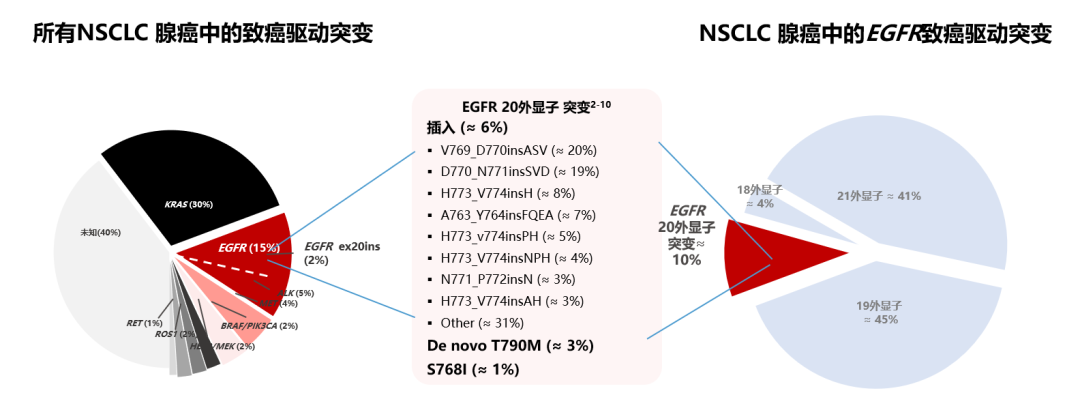
图2. EGFR突变和 EGFR ex20ins的分布[2-11]
受限于检测水平,临床上EGFR ex20ins患者可能远比文献报告的比例要高。
与EGFR经典突变相比,EGFR ex20ins患者的预后更差
表现1:生存期短,比常见EGFR突变生存期短
一项入组3014例EGFR突变NSCLC患者的回顾性真实世界队列研究的结果显示,EGFR ex20ins和常见EGFR患者的5年真实世界总生存(rwOS)率分别为8%和19%;中位rwOS分别为16.2个月(95% CI,11.04-19.38个月),和25.5个月(24.48-27.04)[调整后 HR=1.75 (1.45-2.13);P<0.0001] [12]。
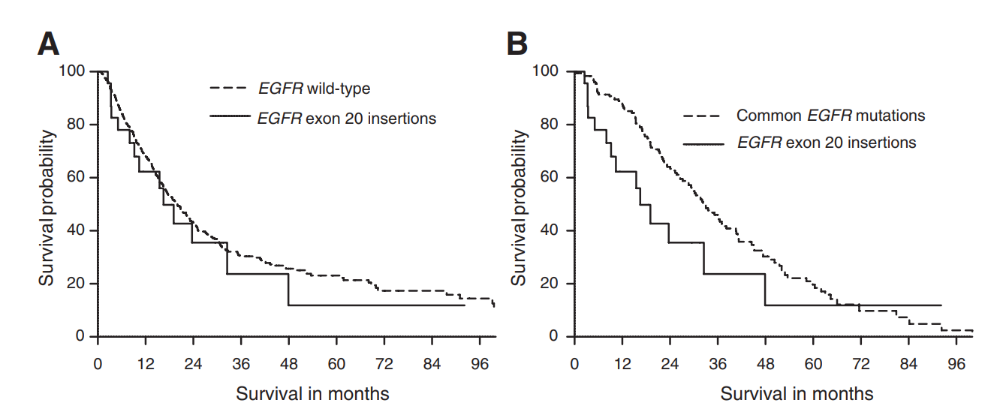
另一项队列研究中,入组了1086例EGFR分型的受试者,结果同样表明:EGFR ex20ins患者(16.5个月)的与野生型患者(20.0个月)的生存期相似,但比常见EGFR突变肺癌(33.0个月)的生存期短[13] (图3)。
表现2:死亡风险高
从2022年ELCC大会上的一项韩国大样本的回顾性研究中,分析了EGFR 20ins患者53例(2.4%),其中62.3%接受了一线含铂化疗,24.5%接受了一线TKI治疗。结果显示,不论是一线含铂化疗还是一线TKI治疗,EGFR ex20ins NSCLC患者的疗效并不理想,EGFR exon 20ins NSCLC患者的死亡风险是EGFR常见突变患者的两倍(HR=2.16;P<0.001)[14]。
表现3:至停药时间(TTD)和至下次治疗时间(TTNT)短
在上面提及的韩国回顾性研究中,数据同样显示,TTD(HR=2.47;p < 0.001)和TTNT(HR=4.32;p < 0.001)也显著更短[14]。
EGFR ex20ins患者目前的治疗现状如何?
现状1:EGFR ex20ins亚型多样,对传统EGFR-TKI的治疗疗效存在异质性[15]
EGFR ex20ins有多种插入亚型,不同亚型对治疗的敏感性不同。可根据结构分为四个亚组,用于预测EGFR-TKI疗效[15](图4)。
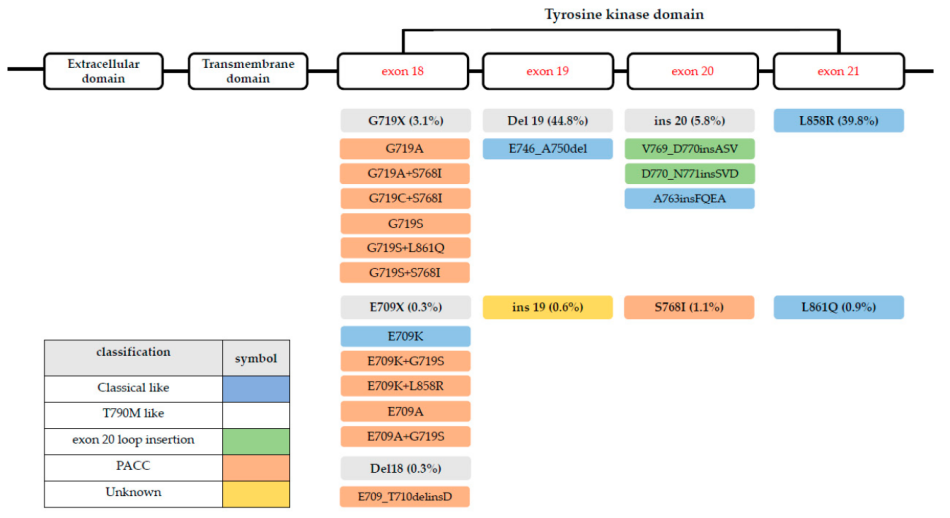
图4. EGFR ex20ins有多种插入亚型,不同亚型对治疗的敏感性不同
这种分类方法可以更好地根据药物敏感性定义突变组:
经典样突变对所有三代EGFR-TKI都敏感;
α-C螺旋内(氨基酸761-766):插入亚型对已获批的EGFR抑制剂敏感(如A763_Y764insFQEA),Loop环区内插入突变则治疗疗效较差;
P环近端结构区内的插入突变类型的缓解率高于P环远端插入类型。
现状2:存在与EGFR ex20ins突变检测相关的问题
基因检测是NSCLC治疗管理的关键环节,确切识别特异性序列亚型尤为重要。然而EGFR ex20ins由于插入的多样性和复杂的结构,检测率很低。
最常用的检测手段包括聚合酶链反应(PCR)和下一代测序(NGS)等。其中,PCR易漏检,需要相对较大的组织样本,在EGFR ex20ins等分子异质性突变检测方面能力不足[16]。Foundation Medicine的数据显示,与NGS相比,PCR遗漏了51.4%的突变[17]。
NGS作为识别分子异质性序列改变的诊断工具,敏感性更高,可靠性更强,因而更具价值。尽管作为《二代测序技术在NSCLC中的临床应用中国专家共识(2020版)》优先推荐检测手段,临床实践上NGS在中国EGFR ex20ins NSCLC患者中的应用情况仍不清楚[16]。
现状3:权威指南推荐起始治疗参考无驱动基因的NSCLC系统性治疗策略
化疗仍是全球常用的标准一线治疗。NCCN和CSCO起始治疗参考无驱动基因的NSCLC系统性治疗策略,尚未推荐特异性治疗方案(图5和图6),更多的一线靶向治疗策略仍有待探索。
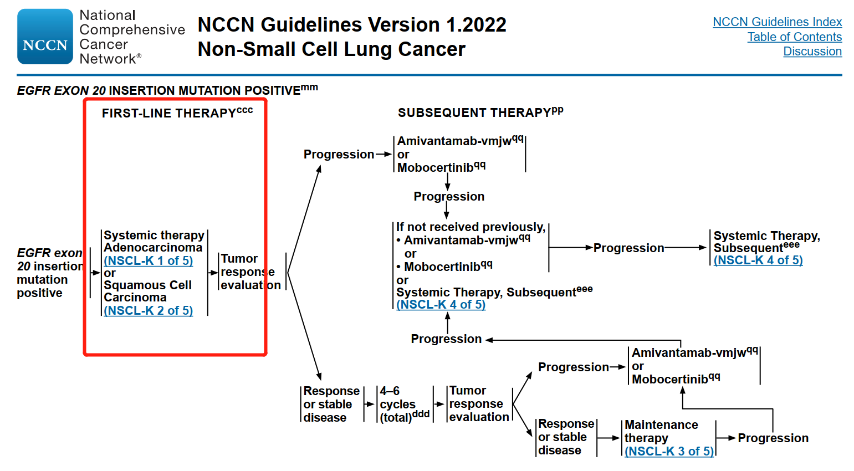
图5. 2022 v1 NCCN 非小细胞肺癌诊疗指南[18]

图6. 2022 CSCO 非小细胞肺癌诊疗指南[19]
既往传统治疗获益有限,目前已出现里程碑式的进步
在有针对性靶向药物问世前,EGFR ex20ins患者能够选择的治疗方案包括化疗、传统EGFR-TKI和免疫治疗。
化疗和免疫肿瘤治疗
化疗及化疗联合方案是EGFR ex20ins NSCLC最常用的一线治疗,但效果并不理想[17]。据美国癌症电子病历FlatironHealth数据库截至2020年2月记录,化疗及化疗联合方案约占全部治疗手段的60%,获得的总缓解率(ORR)接近20%(n=57),中位无疾病进展生存期(PFS)为4.5个月-5.7个月[17]。
免疫肿瘤治疗作为单药一线方案时,确认的ORR仅 为9.1%,PFS为3.1个月(n=11),作为铂类经治后≥二线治疗时,ORR为5.0%,PFS为2.2个月(n=20);传统EGFR-TKI作为单药一线方案时,ORR仅为2.7%,PFS为3.3个月(n=37),作为铂类经治后≥二线治疗时,ORR为10.0%,PFS为3.4个月(n=10)[17]。
传统EGFR-TKI
在一项真实世界数据meta分析结果显示:EFGR-TKI用于一线治疗汇总估计的PFS为3.0个月(95% C1:2.0,3.8),OS则为16.4个月(95% Cl:1.6,19.7);EFGR-TKI用于后线治疗汇总估计的PFS为2.1个月(1.9,3.0),OS为14.1个月(12.9,15.3)[20](表3)。
表3.EGFR-TKI IL和≥2L PFS、OS 的汇总分析

里程碑进展——最新靶向治疗:ORR获得显著提升,mOS超过2年[17]
长期以来,化疗、传统EGFR-TKI、免疫肿瘤治疗等方案获益有限,患者生存结局差,EGFR ex20ins NSCLC患者治疗面临着相当大的挑战。
现在相对成熟的针对EGFR ex20ins的靶向药物包括:Mobocertinib(莫博赛替尼)和Amivantamab,它们于2020年被美国FDA授予突破性治疗药物资格,用于既往接受含铂化疗时或之后疾病进展的EGFR ex20ins转移性NSCLC成人患者。
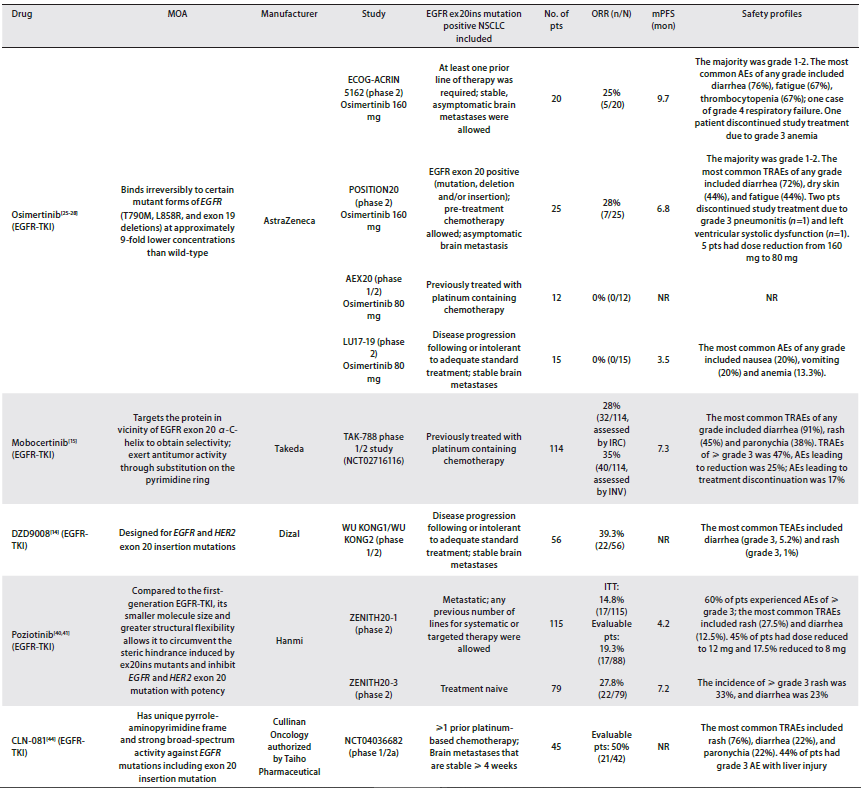
目前研究数据显示,新型靶向药物可使这类患者的ORR获得显著提升,mOS超过2年[17](表4)。
表4. 针对EGFR 外显子20插入突变阳性NSCLC的药物临床数据汇总[20]
小结
总之,EGFR ex20ins NSCLC异质性高、预后差、对传统治疗不敏感,未满足的临床需求很高。近年来,EGFR ex20ins NSCLC靶向治疗出现了里程碑式的进步,包括首个特异性设计的新型EGFR-TKI 莫博赛替尼和EGFR/MET双特异性抗体Amivantamab等获得美国FDA批准以及NCCN指南推荐,在样本量相对较大(莫博赛替尼研究N=114,Amivantamab研究N=81)的EGFR ex20ins NSCLC中证实带来临床意义上的持续缓解,为患者创造了更多可能的治疗选择。
参考文献:
[1].Fang W, Huang Y, Hong S, et al. EGFR exon 20 insertion mutations and response to osimertinib in non-small-cell lung cancer[J]. BMC Cancer, 2019, 19(1):595
[2].Chan BA, Hughes BG. Targeted therapy for non-small cell lung cancer: current standards and the promise of the future. Transl Lung Cancer Res. 2015;4(1):36-54. doi:10.3978/j.issn.2218-6751.2014.05.01
[3].Oxnard GR, Lo PC, Nishino M, et al. Natural history and molecular characteristics of lung cancers harboring EGFR exon 20 insertions. J Thorac Oncol. 2013;8(2):179-184. doi:10.1097/JTO.0b013e3182779d18
[4].Chong CR, Jänne PA. The quest to overcome resistance to EGFR-targeted therapies in cancer. Nat Med. 2013;19(11):1389-1400. doi:10.1038/nm.3388
[5].Crossland V, et al.The Frequency and Spectrum of EGFR Exon 20 Insertions in NSCLC: A Global Literature Review.J Thorac Oncol 2018;13(10 suppl):S612-S613;
[6].Gazdar AF, Minna JD. Inhibition of EGFR signaling: all mutations are not created equal. PLoS Med. 2005;2(11):e377. doi:10.1371/journal.pmed.0020377
[7].Gazdar AF. Activating and resistance mutations of EGFR in non-small-cell lung cancer: role in clinical response to EGFR tyrosine kinase inhibitors. Oncogene. 2009;28 Suppl 1(Suppl 1):S24-S31. doi:10.1038/onc.2009.198
[8].Jorge SE, Kobayashi SS, Costa DB. Epidermal growth factor receptor (EGFR) mutations in lung cancer: preclinical and clinical data. Braz J Med Biol Res. 2014;47(11):929-939. doi:10.1590/1414-431X20144099
[9].Kobayashi Y, Mitsudomi T. Not all epidermal growth factor receptor mutations in lung cancer are created equal: Perspectives for individualized treatment strategy. Cancer Sci. 2016;107(9):1179-1186. doi:10.1111/cas.12996
[10].Lee JK, Shin JY, Kim S, et al. Primary resistance to epidermal growth factor receptor (EGFR) tyrosine kinase inhibitors (TKIs) in patients with non-small-cell lung cancer harboring TKI-sensitive EGFR mutations: an exploratory study. Ann Oncol. 2013;24(8):2080-2087. doi:10.1093/annonc/mdt127
[11].Arcila ME, Nafa K, Chaft JE, et al. EGFR exon 20 insertion mutations in lung adenocarcinomas: prevalence, molecular heterogeneity, and clinicopathologic characteristics. Mol Cancer Ther. 2013;12(2):220-229. doi:10.1158/1535-7163.MCT-12-0620
[12].Bazhenova L, Minchom A, Viteri S, Bauml JM, Ou SI, Gadgeel SM, Trigo JM, Backenroth D, Li T, Londhe A, Mahadevia P, Girard N. Comparative clinical outcomes for patients with advanced NSCLC harboring EGFR exon 20 insertion mutations and common EGFR mutations. Lung Cancer. 2021 Dec;162:154-161. doi: 10.1016/j.lungcan.2021.10.020. Epub 2021 Nov 6. PMID: 34818606.
[13].Oxnard GR, Lo PC, Nishino M, et al. Natural history and molecular characteristics of lung cancers harboring EGFR exon 20 insertions. J Thorac Oncol. 2013 8(2):179-184. doi:10.1097/JTO.0b013e3182779d18
[14].Yoon S, Lim SM, Jung HA, et al. Clinical Characteristics, Treatment Patterns and Outcomes of EGFR exon 20 insertion and other EGFR mutations in Korean aNSCLC Patients. 2022 ELCC 50P.
[15].Hou J, Li H, Ma S, et al. EGFR exon 20 insertion mutations in advanced non-small-cell lung cancer: current status and perspectives. Biomark Res. 2022 Apr 13;10(1):21. doi: 10.1186/s40364-022-00372-6.
[16].Kwon CS, Lin HM, Crossland V, et al. Non-small cell lung cancer with EGFR exon 20 insertion mutation: a systematic literature review and pooled analysis of patient outcomes [published online ahead of print, 2022 May 27]. Curr Med Res pin. 2022;1-34. doi:10.1080/03007995.2022.2083326
[17].Kitadai R, Okuma Y. Treatment Strategies for Non-Small Cell Lung Cancer Harboring Common and Uncommon EGFR Mutations: Drug Sensitivity Based on Exon Classification, and Structure-Function Analysis. Cancers (Basel). 2022;14(10):2519. doi: 10.3390/cancers14102519
[18].NCCN Clinical Practice Guidelines in Oncology-Non-small cell lung cancer, version 2[J]. J Natl Compr Canc Netw, 2021
[19].中国临床肿瘤学会指南工作委员会.2022 CSCO非小细胞肺癌诊疗指南[J].人民卫生出版社.
[20].杨雪, 赵军. EGFR外显子20插入突变阳性NSCLC治疗的临床研究进展[J]. 中国肺癌杂志, 2022, 25(5):14.
审批编号:VV-MEDMAT-71717
获批日期:2022 年 7 月
声明:
本资讯旨在帮助医疗卫生专业人士更好地了解相关疾病领域最新进展。本站对发布的资讯内容,并不代表同意其描述和观点,仅为提供更多信息。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
仅供医疗卫生专业人士为了解资讯使用。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解资讯以外的目的,武田不承担相关责任。
截至2022年7月28日,Mobocertinib(莫博赛替尼)尚未获得中国国家药品监督管理局(NMPA)批准,以上信息仅供医疗卫生专业人士了解学术进展使用,武田公司不推荐说明书外应用。
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |