*仅供医学专业人士阅读参考
延长辅助内分泌治疗在激素受体阳性早期乳腺癌治疗中的获益分析。
对于早期激素受体(HR)阳性乳腺癌,辅助内分泌治疗(标准时长5年[1])具有重要作用。最新的研究进展表明延长辅助内分泌治疗时长可能会优化部分患者的治疗疗效,近些年延长辅助内分泌治疗的策略也逐渐被临床医师接受和采用。但关于哪些患者需要延长辅助内分泌治疗,以及延长辅助内分泌治疗的最佳时长等问题,仍存在较多争议[2]。2022年欧洲肿瘤内科学会(ESMO)公布了DATA研究的更新结果(摘要号:133O)[3],为绝经后HR阳性早期乳腺癌患者的辅助内分泌治疗策略提供了思路。同时近期发表的一项真实世界研究也针对延长辅助内分泌治疗的获益人群以及预后相关性等进行了探索[4],医学界肿瘤频道特邀湖南省肿瘤医院刘莉萍教授针对相关研究进展进行解读。
DATA研究最终分析结果提示高风险绝经后HR阳性早期乳腺癌延长辅助内分泌治疗获益显著
DATA研究设计
DATA研究是一项前瞻性、随机、开放标签的Ⅲ期临床试验,2006年6月~2009年8月在荷兰79家中心入组1912例绝经后HR阳性早期乳腺癌患者。符合入组标准的患者在服用他莫昔芬2-3年辅助治疗后,如无复发转移则按照1∶1随机分配至阿那曲唑治疗3年组或6年组。分层因素包括:淋巴结状态、HR状态、HER2状态和他莫昔芬(TAM)持续治疗时间。主要终点为调整的无病生存期(DFS),定义为随机化3年后的DFS。次要研究终点为调整的总生存期(OS)。

图1. DATA研究设计
既往研究结果[5]
早在2017年10月11日,Lancet Oncology就曾在线发表DATA研究成果。2006年6月28日至2009年8月10日期间,入组的1912例患者中,955例分配至阿那曲唑治疗3年组,957例分配至阿那曲唑治疗6年组。其中共1860例符合条件的患者(6年组931例,3年组929例)。中位随访4.2年时,6年组的5年调整的DFS率为83.1% ,3年组为79.4%(HR=0.79,95%CI 0.62-1.02,p=0.066)。随机分组前3年,各组的不良事件发生率没有差异。在整个观察期(0~6年),与3年治疗组相比,6年治疗组的所有等级关节痛或肌痛(6年组58% vs 3年组53%)和骨质疏松症(21% vs 16%)的发生率更高。无论是3年或者6年,各组的心血管不良事件无差异。观察到的不良事件主要为1-2级,未观察到中毒死亡病例。
2022年ESMO更新数据解读
本次ESMO大会公布了最终的分析结果。更新的研究结果表明,主要研究终点aDFS, 阿那曲唑治疗6年组与3年组相比:10年调整的的DFS率分别为69.1%和66%(HR=0.86,95%CI 0.72-1.01,P=0.073),aDFS的绝对获益为3.1%。
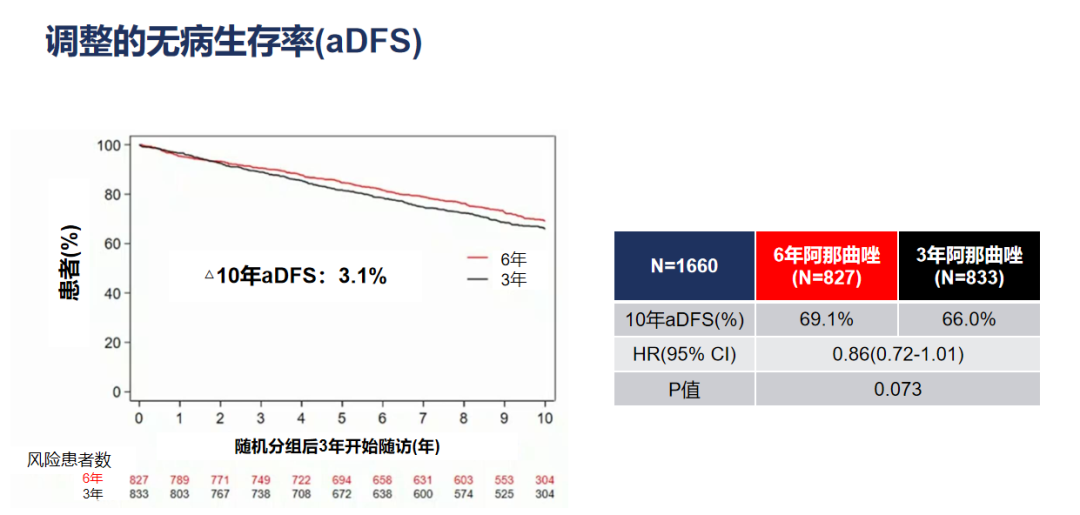
图2. 调整的DFS获益
进一步亚组分析显示,阿那曲唑治疗6年组与3年组相比:
雌激素(ER)阳性且孕激素(PR)阳性:10年调整的DFS率较高(70.8% vs 64.4%,HR=0.77,95%CI 0.63-0.94,P=0.008);
ER阳性或PR阳性:10年调整的DFS率相似(63.7% vs 70.9%,HR=1.22,95%CI 0.86-1.73,P=0.28)。
ER、PR双阳性与单阳性人群相比,延长内分泌治疗组的10年调整的DFS率显著更优(交互P=0.018)。
此外,对于淋巴结阳性且ER、PR双阳性患者(849例),阿那曲唑治疗6年组与3年组相比,10年调整的DFS率显著较高(68.7% vs 60.7%,HR=0.74,95%CI 0.59-0.93,P=0.011);对于淋巴结阳性、肿瘤≥2厘米且ER、PR双阳性患者(429例),阿那曲唑治疗6年组与3年组相比,10年调整的的DFS率显著较高(70.0% vs 56.4%,HR=0.64,95%CI 0.47-0.88,P=0.005)。


图3、图4. 亚组患者的DFS获益
在次要研究终点方面,阿那曲唑治疗6年组与3年组相比:10年调整的的OS率分别为80.9%和79.2%(HR=0.93,95%CI 0.75-1.16,P=0.53),OS的绝对获益为1.7%。
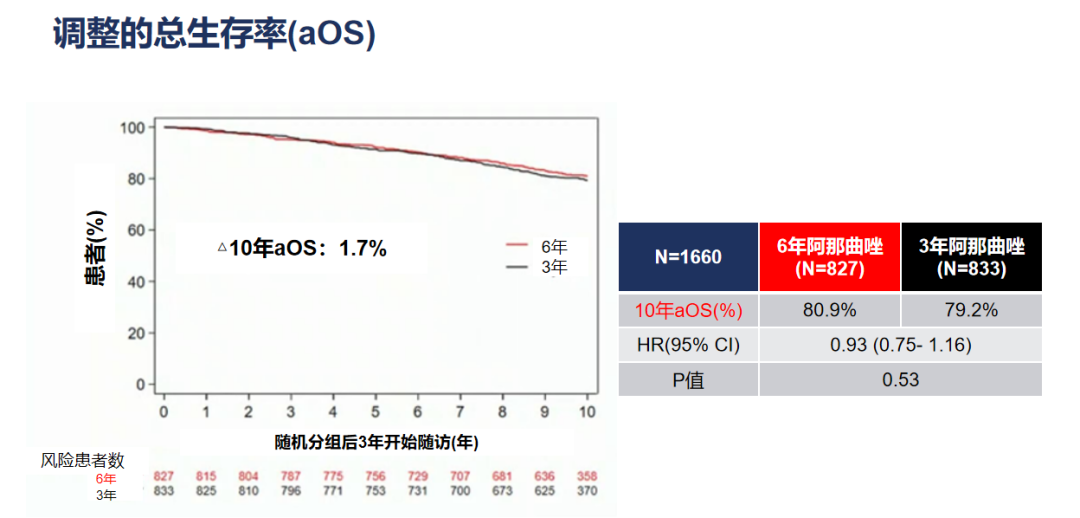
图5. 调整的OS获益
进一步亚组分析显示,阿那曲唑治疗6年组与3年组相比:
ER阳性且PR阳性:10年调整的OS率两组分别为82.7% vs 78.7%(HR=0.83,95%CI 0.65-1.07)。
ER或PR阳性:10年调整的OS率两组分别为75.2% vs 81.0%(HR=1.33,95%CI 0.86-2.05)。
对于淋巴结阳性且ER、PR双阳性患者,阿那曲唑治疗6年组与3年组相比,10年调整的OS率分别为81.4%和76.7%(HR=0.84,95%CI 0.62-0.93,P=0.23);对于淋巴结阳性、肿瘤≥2厘米且ER、PR双阳性患者,阿那曲唑治疗6年组与3年组相比,10年调整的OS率分别为80.6%和72.5%(HR=0.71,95%CI 0.48-1.05,P=0.084)。


图6、图7. 亚组患者的OS获益
研究结论
不建议对所有绝经后HR阳性乳腺癌患者采用芳香化酶抑制剂序贯辅助内分泌治疗长达5年以上。ER、PR双阳性可有效预测延长治疗的疗效并指导临床决策,同时可根据诸如淋巴结状态、肿瘤大小等解剖学因素筛选最能从延长内分泌治疗中获益的人群。
真实世界研究揭示延长辅助内分泌治疗的决定因素和有效性
研究简介
本研究使用了瑞典6个健康登记处的数据,以患者为基础,旨在
评估延长辅助内分泌治疗的发生情况及其随时间的变化;
确定决定使用延长辅助内分泌治疗的临床特征和患者因素;
在真实世界中探索延长辅助内分泌治疗与生存结局之间的相关性。
研究前瞻性随访了13168例乳腺癌患者(2005-2020年),从他们首次处方他莫昔芬或芳香化酶抑制剂开始,并将他们归类为延长或不延长辅助内分泌治疗。Cox回归分析用于评估延长辅助内分泌治疗是否与乳腺癌结局相关。延长辅助内分泌治疗定义为继续治疗≥6个月,并在5年辅助内分泌治疗后登记≥2次他莫昔芬或芳香化酶抑制剂处方。他莫昔芬或芳香化酶抑制剂处方信息来自瑞典处方药登记处。
研究结果
1.10年内辅助内分泌治疗的使用情况在完成5年辅助内分泌治疗的4660例患者中,1386例(29.7%)患者延长了治疗。与此一致,在完成前5年辅助内分泌治疗后6个月内,继续使用辅助内分泌治疗的患者从57.7%急剧下降至20.0%。
2.延长辅助内分泌治疗的发生情况在过去10年中,延长治疗的患者比例急剧增加。在符合临床指南延长治疗标准的患者中,相应比例从2010-2011年的16.7%增加至2018-2020年的80.9%。在不符合延长治疗标准的患者中,相应比例也增加了近5倍,从2010-2011年的8.1%增加至2018-2020年的39.6%。
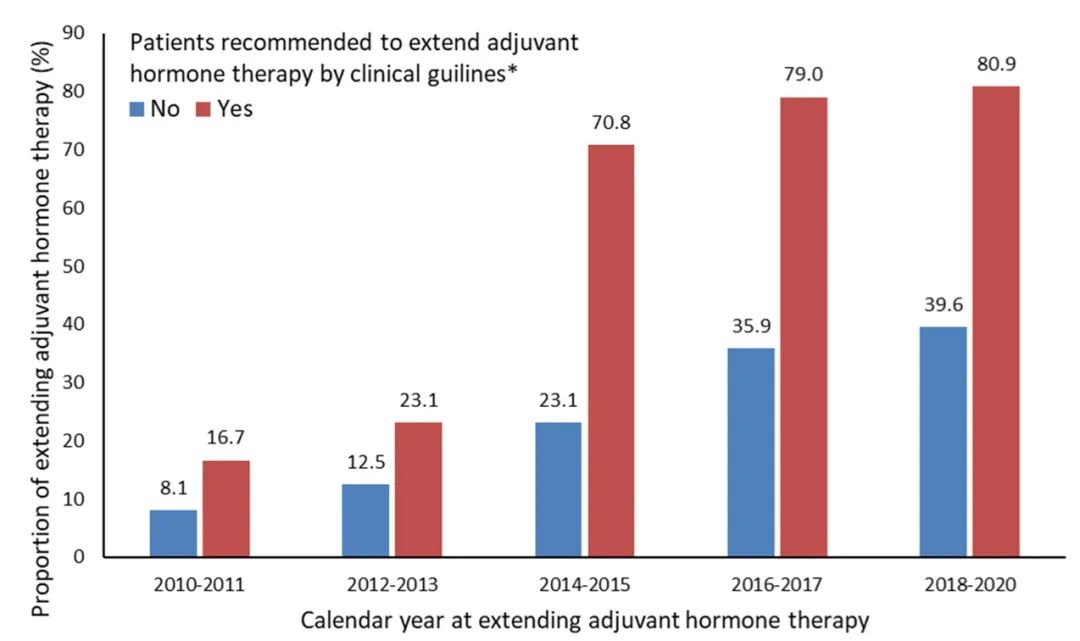
图8. 根据2010-2020年瑞典国家临床指南是否建议延长治疗,确定完成5年辅助内分泌治疗的患者延长治疗的发生情况
3.延长辅助内分泌治疗的预测因素诊断时年龄较小、使用芳香化酶抑制剂(与他莫昔芬相比)、肿瘤体积较大、淋巴结受累阳性、肿瘤分级较高、孕激素受体状态阴性、HER2状态阳性、化疗、放疗、一级亲属死于乳腺癌、高收入的患者群体,在年龄调整模型中,与完成5年辅助内分泌治疗后延长治疗的更高可能性相关。
在多变量校正模型中,诊断时年龄较小(< 40 vs ≥65岁)、淋巴结受累阳性、肿瘤分级较高(3级 vs 1 级)、化疗、一级亲属死于乳腺癌、高收入与延长辅助内分泌治疗的相关性仍具有统计学意义。
4.延长辅助内分泌治疗与生存结局的相关性在未延长辅助内分泌治疗的患者中,DFS分析的事件发生率为26.8(95%CI,24.2-29.8)/1000人-年,在完成5年辅助内分泌治疗后延长治疗的患者中为20.6(95%CI,16.6-25.6)/1000人-年。Cox回归分析显示辅助内分泌治疗的时间延长与DFS改善相关(DFS事件发生的HR=0.72,95 CI% 0.55-0.95)。然而,当比较辅助内分泌治疗的延长者与非延长者时,未发现OS的统计学显著差异(HR=0.94,95 CI% 0.67-1.33)。按基线时肿瘤大小、淋巴结状态、肿瘤分级或辅助内分泌治疗类型进行的亚组分析显示了一致的结果。

图9. 延长辅助内分泌治疗和未延长辅助内分泌治疗患者的DFS和OS
研究总结与讨论
该研究发现,在过去的几十年中,无论是符合还是不符合临床指南的延长标准,延长辅助内分泌治疗的女性比例都增加了5倍。肿瘤特征较差(淋巴结阳性、肿瘤分级高)、接受化疗或一级亲属死于乳腺癌的患者更有可能延长辅助内分泌治疗至5年以上。延长的辅助内分泌治疗与更好的DFS获益相关。
自2010年以来,临床指南建议淋巴结阳性的他莫昔芬使用者接受延长治疗[6-8]。在该研究中,2019年近90%淋巴结阳性的他莫昔芬使用者接受了延长治疗,提示对临床指南的依从性相对较好。自2018年以来,临床指南建议芳香化酶抑制剂使用者延长治疗[9,10]。然而,2017年,就有71%的淋巴结阳性疾病患者在5年芳香化酶抑制剂治疗后延长了辅助内分泌治疗时间。这表明已有证据和临床指南之间存在时间滞后,临床医生可能已经根据他们的认知为芳香化酶抑制剂使用者处方了延长治疗[11-14]。
研究中,接受化疗的乳腺癌患者接受延长辅助内分泌治疗的可能性是未接受化疗患者的5倍以上。接受化疗反映了较差的肿瘤特征,如淋巴结阳性、肿瘤体积大、增殖率高和/或 HER2 状态阳性[15]。该结果与目前的临床指南一致,即仅推荐具有高复发风险的患者接受延长的辅助内分泌治疗[9,10]。
一级亲属死于乳腺癌的乳腺癌患者延长辅助内分泌治疗至5年以上的几率高达84%。预计这些患者通常具有高度积极性,因此可能更愿意延长治疗时间。年轻女性延长辅助内分泌治疗的比例较高,与这些女性患者预后较差相关[16,17]。高等教育和收入也能增加延长辅助内分泌治疗的患者比例。总的来说,该研究表明,疾病严重程度和患者特征都可能影响延长辅助内分泌治疗的决定。
此外,研究中观察到延长辅助内分泌治疗的患者DFS率改善了28%,与临床试验中观察到的效应相当。该研究还表明,在完成5年芳香化酶抑制剂治疗的患者中,延长辅助内分泌治疗与DFS改善相关。总之,该研究从真实世界研究角度说明,延长辅助内分泌治疗超过5年可能改善乳腺癌生存结局。
不过需要指出的是,虽然延长辅助内分泌治疗与乳腺癌事件风险降低相关,但也可能增加其他疾病风险,如心血管疾病和骨折[18]。因此,可能不建议所有乳腺癌患者接受延长辅助内分泌治疗。
总结
DATA研究和真实世界研究数据共同表明,符合临床指南和不符合临床指南延长治疗标准的患者中,辅助内分泌治疗延长至5年以上的患者比例增加。其中,DATA研究还确定了对于ER、PR双阳性人群等,延长辅助内分泌治疗可显著提高获益。当然,对于确定延长辅助内分泌治疗的患者的可能获益因素仍然需要进一步验证。
专家简介

刘莉萍 教授
湖南省肿瘤医院乳腺内科 主任医师
湖南省肿瘤医院乳腺癌多学科会诊组成员
湖南省健康管理学会乳腺甲状腺健康管理专业委员会副主任委员
湖南省妇幼保健与优生优育协会生育力保护与保存专业委员会副主任委员
湖南省国际医学交流促进会乳腺癌专业委员会副主任委员
湖南省预防医学会乳腺疾病防治专业委员会常委
中国女医师协会乳腺专业委员会常委
长江学术带乳腺联盟常委
湖南省妇幼保健与优生优育协会妇科与乳腺肿瘤防治专业委员会委员
湖南省抗癌协会分子靶向治疗专业委员会委员
湖南省医学会乳腺癌规范化诊治专家巡讲团成员
参考文献:
[1].2022年CSCO乳腺癌诊疗指南
[2].周易, 刘晓安. 早期乳腺癌延长内分泌治疗的研究进展[J]. 中国肿瘤外科杂志, 2022(014-002).
[3].Tjan-Heijnen VCG, Lammers SWM, Geurts SME, et al. Extended adjuvant aromatase inhibition after sequentialendocrine therapy: Final results of the phase III DATA trial. 2022 ESMO abstract 133O.
[4].Zeng E, He W, Sjölander A, et al. Determinants and effectiveness of extending the duration of adjuvant hormone therapy beyond 5 years in breast cancer patients. Cancer Res. 2022 Aug 18:CAN-22-0900.
[5].Tjan-Heijnen VCG, van Hellemond IEG, Peer PGM, et al; Dutch Breast Cancer Research Group (BOOG) for the DATA Investigators. Extended adjuvant aromatase inhibition after sequential endocrine therapy (DATA): a randomised, phase 3 trial. Lancet Oncol. 2017 Nov;18(11):1502-1511.
[6].Breast cancer National care program. Regional Cancer Center; 2009.
[7].Aebi S, Davidson T, Gruber G, et al. Primary breast cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of oncology : official journal of the European Society for Medical Oncology 2010;21 Suppl 5:v9-14.
[8].Burstein HJ, Prestrud AA, Seidenfeld J, et al. American Society of Clinical Oncology clinical practice guideline: update on adjuvant endocrine therapy for women with hormone receptor-positive breast cancer. Journal of clinical oncology : official journal of the American Society of Clinical Oncology 2010;28:3784-96.
[9].Burstein HJ, Lacchetti C, Anderson H, et al. Adjuvant Endocrine Therapy for Women With Hormone Receptor-Positive Breast Cancer: ASCO Clinical Practice Guideline Focused Update. Journal of clinical oncology : official journal of the American Society of Clinical Oncology 2019;37:423-38.
[10].Breast cancer National care program. Regional Cancer Center; 2018.
[11].Goss PE, Ingle JN, Pritchard KI, et al. Extending aromatase-inhibitor adjuvant therapy to 10 years. The New England journal of medicine. 2016;375:209-19.
[12].Tjan-Heijnen VCG, van Hellemond IEG, Peer PGM, et al. Extended adjuvant aromatase inhibition after sequential endocrine therapy (DATA): a randomised, phase 3 trial. Lancet Oncol 2017;18:1502-11
[13].Mamounas EP, Bandos H, Lembersky BC, et al. Use of letrozole after aromatase inhibitor-based therapy in postmenopausal breast cancer (NRG Oncology/NSABP B-42): a randomised, double-blind, placebo-controlled,phase 3 trial. The Lancet Oncology 2019;20:88-99.
[14].Del Mastro L, Mansutti M, Bisagni G, et al.Extended therapy with letrozole as adjuvant treatment of postmenopausal patients with early-stage breast cancer: a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2021;22:1458-67.
[15].Burstein HJ, Curigliano G, Loibl S, et al.Estimating the benefits of therapy for early-stage breast cancer: the St. Gallen International Consensus Guidelines for the primary therapy of early breast cancer 2019. Annals of Oncology 2019;30:1541-57.
[16].Bharat A, Aft RL, Gao F, Margenthaler JA. Patient and tumor characteristics associated with increased mortality in young women (< or =40 years) with breast cancer. Journal of surgical oncology 2009;100:248-51.
[17].Azim HA, Jr., Partridge AH. Biology of breast cancer in young women. Breast Cancer Res 2014;16:427.
[18].Goldvaser H, Barnes TA, Šeruga B, et al.Toxicity of Extended Adjuvant Therapy With Aromatase Inhibitors in Early Breast Cancer: A Systematic Review and Meta-analysis. JNCI: Journal of the National Cancer Institute 2017;110:31-9.
审批编号:CN-103220 Expiration Date: :2023-9-23
材料由阿斯利康提供,仅供医疗卫生专业人士参考


| 留言与评论(共有 0 条评论) “” |