*仅供医学专业人士阅读参考
解读一例存在EML4-ALK BIRC6-ALK双融合的NSCLC患者的诊疗经过。
肺癌是最常见的恶性肿瘤之一,非小细胞肺癌(NSCLC)占肺癌的80%-85%,随着NSCLC发病机制研究的不断深入和驱动基因的发现,靶向治疗显著改善驱动基因阳性晚期NSCLC的预后[1]。ALK融合作为NSCLC重要的驱动基因,此部分患者可以从ALK抑制剂治疗中获益。ALK融合存在多种伴侣基因,除了常见的EML4-ALK之外,越来越多的少见融合伴侣被报道,临床治疗中对于ALK罕见融合NSCLC患者治疗的关注度逐步提升。
不断探索新的ALK融合形式,研究其与药物敏感性的相关性,具有重要的临床意义。目前在NSCLC中已发现了90多种较罕见的ALK融合,包括KIF5B-ALK,HIP1-ALK,TPM-3ALK等[2,3]。2020年,Lung Cancer杂志报告了一例患者存在EML4-ALK BIRC6-ALK双融合,并对二代ALK-TKI敏感[4]。
EML4-ALK BIRC6-ALK双融合患者对阿来替尼敏感
患者为60岁男性,2019年12月例行体检,CT显示右上肺前段一个大小为2.3 cm x 3.1 cm的肿块,合并双肺多发转移,以及纵隔淋巴结转移。经过肺部活检,病理诊断为右肺腺癌(T4N3M1a, IVA期)。
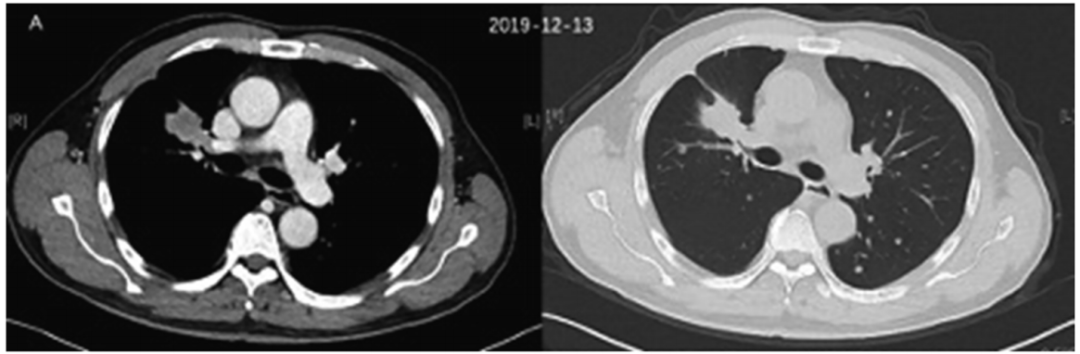
图1. 2019年12月CT检查结果
NGS显示存在ALK双融合突变:EML4-ALK(E20: A20,在组织中丰度为2.14%)和BIRC6-ALK(A19: B33,在组织中丰度为3.42%)。2020年1月起,患者开始口服阿来替尼,剂量为600mg,每日2次。阿来替尼治疗2个月后,2020年3月CT复查发现病灶从2.3 cm × 3.1 cm缩小至1.7 cm × 2.3 cm。
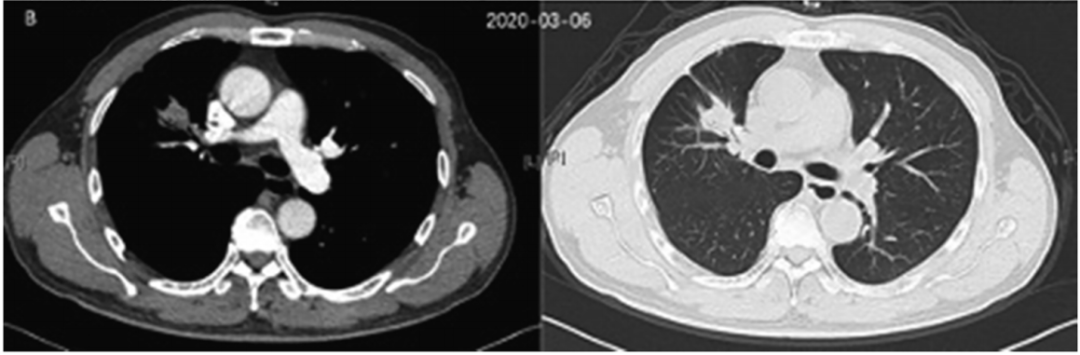
图2. 2020年3月CT检查结果
通过液体活检NGS检测血浆循环肿瘤DNA(ctNDA),发现ALK融合基因消失。截至2020年4月,患者仍在服用阿来替尼,未发现明显的药物相关不良反应。
其他ALK融合对阿来替尼也敏感
既往研究数据显示,一代ALK-TKI药物克唑替尼,及二代ALK-TKI药物布格替尼、塞瑞替尼的疗效可能会受到EML4变体类型的影响,治疗V3变体患者的客观缓解率(ORR)、无进展生存期(PFS)等数据一般较V1变体患者低,例如克唑替尼治疗EML4-ALK V1变体和V3变体的中位PFS分别为11.0个月和4.2个月(P<0.05)[5-8]。阿来替尼在不同的ALK融合突变中展现了较为一致的疗效,BFAST[9]研究结果显示,针对EML4-V1或V3变体的ALK融合患者,阿来替尼均展示了具有一致性的良好应答率,患者的ORR在90%左右。此外,在该研究结果中,阿来替尼在ALK融合伴侣基因非EML4(non-EML4-ALK)患者中也展现了良好的治疗效果,ORR达79%。
而在其他的罕见突变,如HIP1-ALK融合、STRN-ALK融合、LINC00478/LINC01549和ALK外显子20的基因间区域融合的治疗中,阿来替尼也均取得了不错的疗效[10-12]。发表在2021年Lung Cancer中的一个病例显示[10], HIP1-ALK融合可能导致克唑替尼治疗原发耐药,而阿来替尼治疗对克唑替尼原发耐药的HIP1-ALK患者产生持续缓解,中位PFS超过9个月。发表在2020年JTO Clin Res Rep中的一个病例显示[11],STRN-ALK(融合断点S3、A20)融合患者接受阿来替尼治疗连续6个月持续应答,同时无≥2级不良事件发生。发表在2020年JTO Clin Res Rep中的一个病例显示[12],对于发生LINC00478/LINC01549和ALK外显子20的基因间区域融合的患者,阿来替尼同样可以带来临床获益。截止数据提交时,患者接受阿来替尼治疗后的中位PFS已超过6个月。
小结
约5%的肺腺癌中存在ALK基因融合,但ALK双融合的发生率较低,相关数据较少。到目前为止,只有少数病例报告。临床治疗中对于ALK罕见融合的关注度在不断提升,这是第一例报道的EML4-ALK BIRC6-ALK双融合病例,患者通过二代TKI阿来替尼治疗,获得了良好的效果。此外,对于其他罕见融合(如STRN-ALK融合、LINC00478/LINC01549),阿来替尼均取得了不错的疗效。
专家简介

于江泳 教授
肿瘤学博士 博士后 硕士研究生导师 博士后合作导师
北京医院肿瘤科 副主任医师
目前担任北京肿瘤学会肺癌专业委员会常务委员兼秘书,中国临床肿瘤学会(CSCO)肿瘤营养治疗专家委员会委员,中国人体健康科技促进会肿瘤化疗专业委员会委员,北京癌症防治学会肺癌免疫治疗专业委员会委员,北京医学奖励基金会肺癌医学青年专家委员会委员,北京乳腺病防治学会肿瘤免疫治疗专业委员会委员,北京整合医学学会肺癌专业委员会第一届委员,北京抗癌协会科普专业委员会第一届委员等。
主攻专业方向:肺癌精准诊治与个体化治疗。2019年以来主持国家自然科学基金专项项目和国家自然科学基金面上项目各一项,先后参与重大协同创新、国家重点研发计划及国自然重点等多项国家级课题研究工作,先后在CCR、CJC、SCRT、Cancer Lett和Cancer Med等发表SCI论文。
参考文献:
[1].张涛.分子靶向药物应用于非小细胞肺癌维持治疗的研究进展[J].中国肺癌杂志,2010,13(11):1070-1073.
[2].Takita, J. The role of anaplastic lymphoma kinase in pediatric cancers. Cancer Sci 108, 1913-1920. (2017).
[3].Katayama, R. et al. Therapeutic targeting of anaplastic lymphoma kinase in lung cancer: a paradigm for precision cancer medicine. Clin Cancer Res 21, 2227-2235. (2015).
[4].Zhong JM, Zhang GF, Lin L, Li DY, Liu ZH. A novel EML4-ALK BIRC6-ALK double fusion variant in lung adenocarcinoma confers sensitivity to alectinib. Lung Cancer. 2020;145:211-212.
[5].Christopoulos P, Endris V, Bozorgmehr F, et al. EML4‐ALK fusion variant V3 is a high‐risk feature conferring accelerated metastatic spread, early treatment failure and worse overall survival in ALK+ non‐small cell lung cancer[J]. International Journal of Cancer, 2018, 142(12): 2589-2598.
[6].Yoshida T, Oya Y, Tanaka K, et al. Differential crizotinib response duration among ALK fusion variants in ALK-positive non–small-cell lung cancer[J]. Journal of Clinical Oncology, 2016, 34(28): 3383-3389.
[7].Camidge D R, Niu H, Kim H R, et al. Correlation of baseline molecular and clinical variables with ALK inhibitor efficacy in ALTA-1L[J]. Journal of Clinical Oncology, 2020, 38(15_suppl): 9517.
[8].Cha Y J, Kim H R, Shim H S. Clinical outcomes in ALK-rearranged lung adenocarcinomas according to ALK fusion variants[J]. Journal of Translational Medicine, 2016, 14(1): 1-10.
[9].Dziadziuszko R, Mok T, Peters S, et al. Blood First Assay Screening Trial (BFAST) in Treatment-Naive Advanced or Metastatic NSCLC: Initial Results of the Phase 2 ALK-Positive Cohort. J Thorac Oncol. 2021;16(12):2040-2050.
[10].Li M, Tang Q, Chen S, et al. A novel HIP1-ALK fusion variant in lung adenocarcinoma showing resistance to Crizotinib[J]. Lung Cancer, 2021, 151: 98-100.
[11].Nagasaka M, Sarvadevabatla N, Iwata S, et al. STRN-ALK, A Novel In-Frame Fusion With Response to Alectinib. JTO Clin Res Rep. 2020;2(2):100125.
[12].Peng W, Li S, Li L, Xiao M, Zhong J. A Novel LINC00478/LINC01549 Intergenic Region-ALK Fusion Responded Well to Alectinib in a Patient With Lung Adenocarcinoma. JTO Clin Res Rep. 2020;2(1):100112.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |