*仅供医学专业人士阅读参考
EGFR突变阳性肺腺癌经奥希替尼治疗转化为小细胞肺癌或肺鳞癌,该如何应对?
针对EGFR突变阳性晚期非小细胞肺癌(NSCLC),奥希替尼已成为国内外权威指南推荐的一线治疗标准乃至优选方案。然而,在临床实践中,仍有不少临床医生存在顾虑:如果第三代武器先用上了,后面发生耐药后该怎么办?在“好药先行,耐药无忧”系列文章中,我们之前已经对奥希替尼一线治疗后有明确耐药靶点突变时的应对策略进行了介绍,本文将阐述组织学转化导致耐药的发生情况及相应的应对策略。
回顾FLAURA研究数据:
奥希替尼一线治疗优势凸显
Ⅲ期FLAURA研究奠定了奥希替尼在EGFR突变阳性晚期NSCLC一线治疗中的“王者”地位。在无进展生存期(PFS)方面,奥希替尼治疗患者的中位PFS达到18.9个月,相比一代EGFR-TKI显著延长8.7个月[1];在总生存期(OS)方面,奥希替尼组患者中位OS为38.6个月,相比一代EGFR-TKI显著延长6.8个月,刷新了PFS和OS的历史记录[2]。
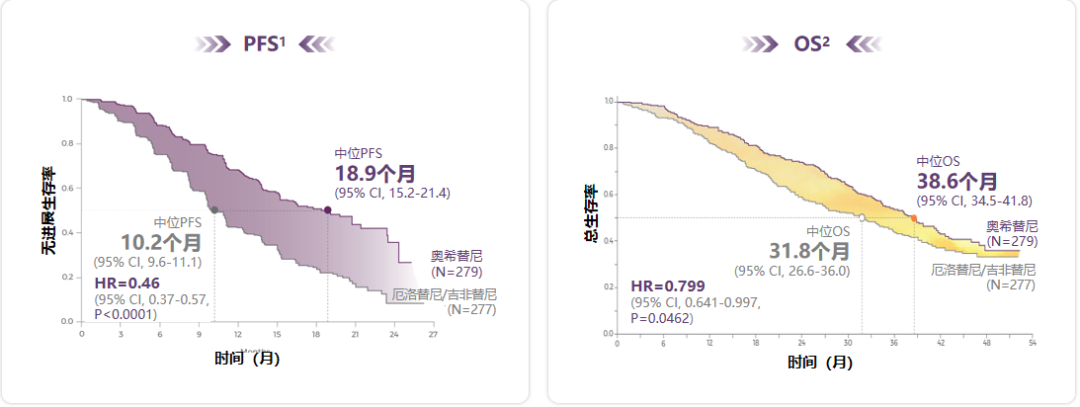
图1.奥希替尼一线治疗的PFS和OS结果
此外,奥希替尼还具有强大的穿透血脑屏障的能力,显著降低基线存在枢神经系统(CNS)转移的患者的CNS进展或死亡风险,并可以减少新发CNS的出现[3,4]。同时,奥希替尼还具有良好的安全性[1,2,5]。在EGFR突变阳性晚期NSCLC一线治疗中,奥希替尼获得了国内外权威指南一致最高级别推荐,具有极高的临床治疗地位。

图2.国内外指南对奥希替尼一线治疗的推荐现状
组织学转化是
EGFR-TKI耐药的重要机制
毫无疑问,将奥希替尼作为EGFR突变阳性晚期NSCLC患者的一线疗法,可以更大限度地延长患者的生存时间,凸显靶向治疗的临床价值。然而,与其他靶向治疗药物一样,奥希替尼最终也会产生耐药的问题。
组织学转化是EGFR-TKI耐药的重要机制之一,包括转化为小细胞肺癌(SCLC)、鳞状细胞癌等。
1
SCLC转化
目前发生组织学转化的机制尚未完全阐明,有研究提示,在组织学转化之前,有可能检测到共存突变基因,如TP53、Rb1和PIK3CA[6-8]。在TP53和Rb1完全失活以及其他基因改变(如高APOBEC改变)的患者中,SCLC转化的风险可能更高[7,8]。此外,一项回顾性研究发现,治疗前Rb1缺失与SCLC转化显著相关,而治疗前TP53和Rb1缺失的患者通常预后更差[9]。
在EGFR突变阳性的肺腺癌患者中,不论是几代EGFR-TKI,耐药后都可能发生SCLC转化,发生率为5%-14%[6,10-14]。近期有研究显示,奥希替尼一线和二线治疗获得性耐药的患者中组织学转化的发生率分别为15%和14%[15]。SCLC转化一般发生在TKI治疗后的14-26个月,中位时间为18个月[11]。虽然大部分SCLC转化的患者仍保留了原有EGFR突变,但转化后EGFR表达水平下降,这可能是转化后肿瘤对EGFR-TKI治疗不敏感的原因[16,17]。
2
鳞状细胞癌转化
奥希替尼一线治疗耐药后鳞状细胞癌转化的发生率为7%,后线治疗则为9%。与SCLC转化一样,鳞状细胞癌转化后患者通常仍保留着原有EGFR突变,但转化后的分子模式目前尚不明确[15]。
EGFR-TKI耐药后发生组织学转化,
该如何应对?
1
SCLC转化
目前关于转化性SCLC的治疗尚缺乏随机对照研究证据,不过已经有一些回顾性研究进行了相关探索,包括化疗、化疗联合EGFR-TKI等;与此同时,诸如免疫治疗联合PARP抑制剂、奥希替尼联合哺乳动物雷帕霉素靶蛋白(mTOR)抑制剂等多项临床试验正在开展中。
依托泊苷+铂类(EP方案)是转化性SCLC治疗的经典方案。一项回顾性研究纳入67例转化性SCLC的患者,其中30%接受过奥希替尼治疗。这些患者中,EP方案是最常用的治疗方案,结果显示,客观缓解率(ORR)为54%,转化后中位OS为10.9个月[6]。
有研究显示,化疗联合EGFR-TKI或贝伐珠单抗治疗SCLC转化的EGFR突变阳性肺腺癌的效果更好。我国学者进行的一项研究回顾性收集了广东省人民医院既往TKI治疗进展后组织活检证实发生SCLC转化的患者,分析发现,与单纯化疗相比,化疗联合EGFR-TKI或贝伐珠单抗治疗可能具有更好的ORR(25% vs 50%)和转化后PFS(3.9个月 vs 6.4个月),转化后OS也展现出延长的趋势(7.1个月 vs 10.7个月)[18]。
目前国内外指南/共识中对转化性SCLC治疗也进行了相关推荐。2022版中国临床肿瘤学会(CSCO)SCLC诊疗指南指出,可根据 EGFR-TKI治疗后进展模式选择相应的转化性SCLC治疗策略。对于EGFR-TKI耐药后出现系统性快速进展的转化性SCLC,可选择标准的SCLC化疗方案;孤立病灶进展的转化性SCLC可采用原EGFR-TKI/或标准的SCLC化疗方案联合局部治疗;系统性缓慢进展的SCLC患者,可采用标准的SCLC化疗方案±EGFR-TKI治疗[19]。
表1. 2022版CSCO SCLC诊疗指南中转化性SCLC治疗推荐
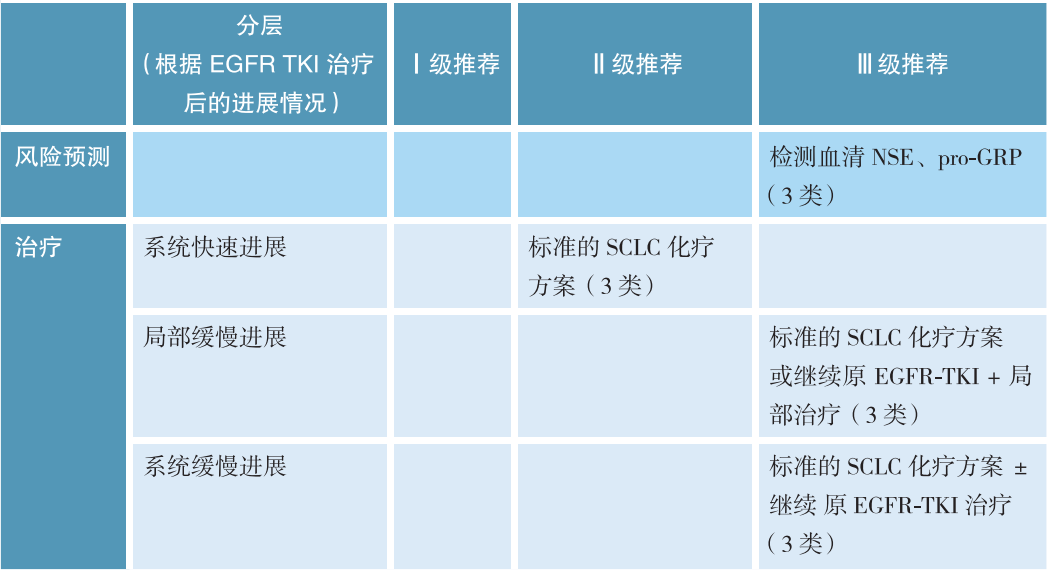
此外,2022版欧洲肿瘤内科学会(ESMO)EGFR突变NSCLC治疗专家共识指出,对于EGFR-TKI耐药后出现SCLC转化的患者,建议使用依托泊苷联合铂类化疗;目前尚不清楚化疗期间是否需要继续使用奥希替尼;对于免疫治疗,则建议参加临床试验[20]。
2
鳞状细胞癌转化
对于鳞状细胞癌转化患者的治疗策略,目前尚缺乏相关研究证据,2022版ESMO EGFR突变NSCLC治疗专家共识中推荐使用适合组织学类型的化疗[20]。
这里分享一则EGFR突变阳性肺腺癌患者奥希替尼获得性耐药后鳞状细胞癌转化的病例:44岁男性非吸烟患者,因“右侧背部疼痛2个月”就诊,确诊为EGFR 19号外显子缺失突变(19del)肺腺癌伴骨转移。吉非替尼治疗10个月后,右肺上叶原发病灶增大。基因检测显示患者存在19del和T790M突变,在采用顺铂+培美曲塞治疗6个周期后,其换用奥希替尼治疗。持续缓解15个月后,患者发生轻微疾病进展,且癌胚抗原(CEA)水平升高,因此加用化疗。然而,右肺上叶的原发肿瘤快速进展,并且出现新发的L3椎体转移。对切除的骨和软组织标本进行病理检测显示组织类型为鳞状细胞癌,基因突变为19del和T790M突变。之后患者接受多西他赛治疗,至病例发表时仍维持疾病稳定[21]。
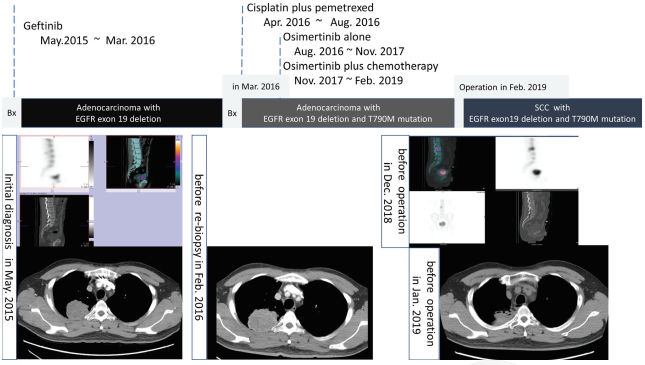
图3. 治疗时间轴以及胸部和骨扫描图片
专家点评:见招拆招,从容应对EGFR-TKI耐药后组织学转化
组织学转化是EGFR-TKI治疗的重要耐药机制之一,不仅可能发生于奥希替尼耐药后,也会发生在一代/二代EGFR-TKI耐药后,因此了解相应的解决方案至关重要。SCLC和鳞状细胞癌是比较常见的组织学转化类型。对于SCLC转化,EP方案是比较常用的治疗方案,并且在化疗的基础上加用EGFR-TKI或抗血管生成治疗可能带来更好的疗效;免疫治疗的疗效尚不确定,目前多项研究正在进行相关探索,希望未来这些研究能够为临床带来更多治疗选择。对于鳞状细胞癌转化,当前尚缺乏相关研究,临床上遇到这种情况时,可按照指南中关于鳞状细胞癌的推荐进行治疗。总之,面对奥希替尼等EGFR-TKI耐药引起的组织学转化,临床医生要见招拆招,从容应对。
专家简介

姚煜教授
西安交通大学第一附属医院
肿瘤内科主任 主任医师 博士生导师
中国临床肿瘤学会(CSCO)理事中华肿瘤康复支持治疗学组副组长
国家肿瘤质控中心肺癌质控专委会委员
国家肿瘤质控中心抗肿瘤监测专委会委员
中国医药教育协会肿瘤化疗专委会副主委
中国医药教育协会肿瘤转移专委会副主委
CSCO恶性黑色素瘤专业委员会常委
CSCO肺癌专业委员会常委
吴阶平肿瘤多学科诊疗委员会常委
陕西省抗癌协会常务理事陕西省抗癌协会化疗专业委员会主任委员
西安市医学会肿瘤学分会主任委员
陕西医学会肿瘤内科专业委员会常委
西安市抗癌学会秘书长
JCO中文编委
参考文献:
[1].Soria et al. N Engl J Med 2018;378:113-25
[2].Suresh S Ramalingam, et al,. N Engl J Med. 2020 Jan 2;382(1):41-50
[3].Reungwetwattana T, et al. J Clin Oncol 2018 Aug 28;JCO2018783118.
[4].2. J Vansteenkiste at ESMO Asia 2017.
[5].Natasha B Leighl, et al,. Eur J Cancer. 2020 Jan;125:49-57.
[6].Marcoux N, et al. J Clin Oncol 2019; 37 (4): 278-285.
[7].Lee JK, et al. J Clin Oncol 2017; 35 (26): 3065-3074.
[8].Offin M, et al. J Thorac Oncol 2019; 14 (10): 1784-1793.
[9].Vokes, N I, et al. J Thorac Oncol. 2022, S1556-0864, 135907.
[10].Oser M G, et al. Lancet Oncol, 2015, 16 (4): el65-el 72.
[11].Sequist LV,et al. Sci Transl Med, 2011, 3 (75): 26r-75r.
[12].Yu ha, et al. Clin Cancer Res, 2013, 19 (8): 2240-2247.
[13].Piotrowska Z, et al. Cancer Discov, 2015, 5 (7): 713-722.
[14].Lee J K, et al. J Clin Oncol, 2017, 35 (26): 3065-3074.
[15].Schoenfeld AJ, et al. Clin Cancer Res. 2020;26(11):2654-2663.
[16].Jiang S-Y, et al. Medicine 2016, 95, e2752.
[17].Niederst MJ, et al. Nat Commun. 2015, 6, 6377.
[18].Zhang C, et al. 2020 WCLC. MA12.08.
[19].2022版中国临床肿瘤学会(CSCO)小细胞肺癌诊疗指南.
[20].Passaro A, et al. Ann Oncol. 2022 ;33(5):466-487.
[21].Zhe-Rong Zheng, et al. Thorac Med 2021; 36: 35-40.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |