
撰文| 李淡宁
#肥胖#
脂肪组织作为一种重要的代谢器官,对能量的吸收、储存、利用、调节及机体能量代谢垃圾的清除等发挥着至关重要的作用。脂肪的正常功能与人类的健康息息相关;尤其是棕色脂肪组织,因其独特的生物学特性,即通过非颤抖产热的形式“燃烧”能量物质,对平衡血液中的血糖、血脂及氨基酸代谢产物发挥了不可替代的作用。近年来的临床数据表明,谁拥有更多的棕色脂肪谁就更健康。然而遗憾的是,通常情况下成年人自身的棕色脂肪组织体积较小而且活力不高。与此同时,工业界开发出的具有降糖降脂的药物总是存在各种各样的副作用。脂肪细胞作为一种重要的分泌器官,那么脂肪细胞自身是否能够分泌脂肪因子 (adpokine),从而激活自身的产热作用,实现“自燃”呢?
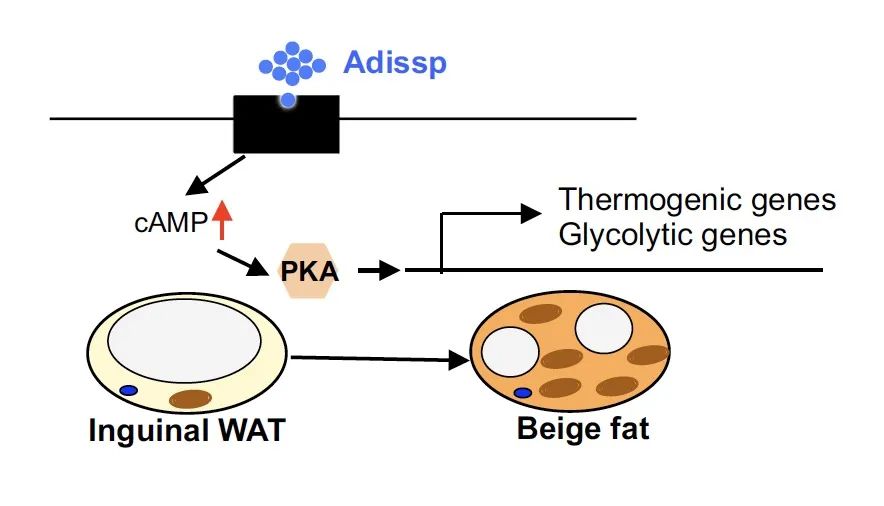
近日,美国马萨诸塞州大学医学院陈庆波、王永旭以article形式在Nature Communications杂志上,在线发表了题为A brown fat-enriched adipokine Adissp controls adipose thermogenesis and glucose homeostasis的文章,报道了棕色脂肪高表达未知脂肪因子、多肽分子Adissp,其不仅能被脂肪细胞以细胞自主的形式大量分泌,同时Adissp亦能以细胞自主的形式有效的激活脂肪细胞自身的产热作用;从而实现降低血糖含量的同时燃烧脂肪细胞内部的脂肪酸。

脂肪细胞的分泌功能极力暗示了其“自燃”的较高可能性,能使脂肪细胞“自燃”的多肽脂肪因子必须具备如下两个条件:1 一般情况下,在棕色脂肪中具有较高的表达水平;2 能被脂肪细胞以细胞自主的方式大量分泌;同时必须能以细胞自主的方式有效激活脂肪细胞自身的产热。本文研究人员采用了不朽的棕色脂肪细胞系,通过收集并分离其培养基中的多肽分子,随后含多肽分子的培养液被用于处理腹股沟白色脂肪组织基质血管部分的原代细胞;试验结果证明多肽分子培养液处理后可使白色脂肪细胞的ucp1 mRNA表达水平升高;这表明棕色脂肪细胞能以细胞自主的方式分泌具有产热作用的多肽分子。通过质谱数据,结合上述条件,最终鉴定到未知脂肪因子, 并命名为Adissp。随后的试验数据表明,Adissp不仅能被棕色脂肪细胞以细胞自主的形式大量分泌,同时能以细胞自主的方式激活脂肪细胞的产热作用。更有趣的是Adissp作为试验用产热明星、临床用受阻的beta肾上腺素受体3的激活小分子,CL 314,243,下游信号效应子;CL 314,243刺激作用极大的加强了breg的分泌;这暗示breg或能弥补beta肾上腺素受体信号的临床局限。
接下来,研究人员在生理条件下深入的探索了Adissp的功能。在以Ap2 (Fapb4) 启动子控制下,构建了脂肪组织中特异过表达Adissp的转基因(Tg)小鼠,同时构建了脂肪组织特异敲除(Adiponectin-Cre, ADKO)小鼠;此外还分别构建了腺病毒表达小鼠及人源Adissp的小鼠。多种模型小鼠的生理数据高度一致的证明,Adissp不仅能够充分的抵抗肥胖,还能有效的降低血糖。值得指出的是,循环系统中,无论是增加小鼠Adissp还是人源的Adissp含量,均能有效降低血糖;这可能基于小鼠与人类Adissp 90.2%的相似性。更重要的是,采用beta肾上腺素受体信号阻断剂处理Adissp转基因小鼠及过表达Adissp的细胞系,Adissp依然能有效的发挥其产热作用。这表明Adissp的产热作用独立于beta肾上腺素受体信号通路。
综上所述,本文文章中的内容虽并未强调脂肪细胞,通过分泌Adissp实现“自燃”;但本文展示的试验数据已经充分证明,在一般条件下,Adissp不仅能被棕色脂肪细胞以细胞自主的方式大量分泌,同时Adissp亦能以细胞自主的方式激活产热相关的信号通路。有趣的是,Adissp作为响应beta肾上腺素受体信号通路的下游效应子,其独立于该信号通路的产热功能将能弥补因这一信号通路相关药物的副作用;不仅如此,本文的数据表明Adissp的产热功能可以不依赖于交感神经系统进行。结合未发表的数据,Adissp的生物学特性高度符合业内人士多年来在寻找的理想产热分子;其对肥胖以及与肥胖相关的代谢疾病的治疗作用值得乐观期待。
原文链接:
https://www.nature.com/articles/s41467-022-35335-w


想了解更多精彩内容,快来关注BioArt生物艺术
| 留言与评论(共有 0 条评论) “” |