*仅供医学专业人士阅读参考
2022年美国临床肿瘤学会(ASCO)年会于6月3日-6月7日芝加哥召开,作为一年一度规模最大的、影响力最大的临床肿瘤学会之一,让我们第一时间浏览本次大会上在前列腺癌领域的最新进展。
Abstract #e17050
ctDNA和肿瘤组织用于检测去势敏感性前列腺癌(CSPC)患者临床相关变异的互补作用
Author:Bin Yang MD, PhD
背景:循环肿瘤细胞DNA(ctDNA)靶向测序在转移性去势抵抗性前列腺癌(mCRPC)患者中已经得到充分研究,在去势敏感性前列腺癌(CSPC)患者中的应用相对有限。此项研究旨在分析ctDNA和匹配组织样本中体系变异的一致性,并探究CSPC患者基因变异的临床意义。
方法:来自中国三家医院的184例CSPC患者,其中有24例局限性前列腺癌(LP)、46例伴淋巴结转移(LNM)、42例伴低肿瘤负荷远处转移(LTB)、72例伴高肿瘤负荷远处转移(HTB)。所有的病人都在初次活检(n=78)或在行根治术(n=106)时同步采集了ctDNA样本和匹配组织样本,用于多基因的高通量靶向测序。选取36个前列腺癌临床相关基因进行分析,通过Kaplan-Meier生存曲线和Cox回归分析,确定基因变异和至CRPC时间的关联。
结果:在全人群中,70.6%的CSPC患者具有肿瘤组织体系变异,远远高于ctDNA的数据占比(31.5%)。在ctDNA和肿瘤组织中检测到的变异一致性为29.2%。在亚组分析中,LP、LNM、LTB和HTB亚组中ctDNA和肿瘤组织中检测到的变异一致性依次为0%、5.3%、3.3%、49.1%。大多数肿瘤组织或ctDNA的变异都显示出其独特性。在肿瘤组织中,LP、LN、LTB和HTB亚组检测到变异数依次为23、54、58、56。而在ctDNA中,变异数则依次为16、27、9、37。ctDNA和肿瘤组织基因变异的综合分析表明,最高频的变异基因是FOXA1(35%)、TP53(16%)、SPOP(12%)、CDK12(12%)、NCOR2(9%)。对于伴有CDK12/TP53/BRCA1/BRCA2/PTEN/RB1等致病性体系或胚系变异的远处转移患者,其进展至CRPC的中位时间明显短于野生型患者(17.3个月vs未达到;p<0.005)。在多变量COX分析中,CDK12/TP53/BRCA1/BRCA2/PTEN/RB1变异仍是有显著性差异的(P=0.00737)。
结论:ctDNA和匹配肿瘤组织的基因变异一致性随CSPC患者疾病进展而增高。单独ctDNA或仅肿瘤组织不足以获取所有临床相关变异,因此组合分析的运用可以为CSPC患者提供更全面的预后和临床治疗指导。CDK12/TP53/BRCA1/BRCA2/PTEN/RB1基因变异是至mCRPC时间的独立预后因子。
Abstract #e17020
中国前列腺癌(PCa)患者基因组全景和同源重组修复(HRR)基因分析
Author:Jianhua Liu
背景:HRR基因突变已被证明为PARP抑制剂(PARPi)治疗转移性去势抵抗性前列腺癌的有效生物标志物。然而,中国人群基因变异流行病学数据和HRR基因变异特征方面的数据仍然不足。
方法:研究收集了250位病理确诊PCa患者的肿瘤组织标本(包括手术和活检标本)和血液标本,并运用二代测序技术(733基因panel)进行分析。肿瘤突变负荷(TMB)定义为体细胞基因编码区非同义突变的总数。同源重组缺陷(HRD)包含杂合性缺失、端粒等位基因不平衡和大区段重组异常三种类型。HRR变异阳性定义为体系或胚系HRR变异(包括拷贝数缺失、拷贝数变异缺失CNV-loss)。
结果:总体来看,体系变异频率最高的3个基因是FOXA1(24.9%)、TP53(15.2%)、MYC(13.6%),而胚系变异频率最高的3个基因则是DPYD(17.1%)、UGT1A1(13.2%)、SLX4(4.3%)。HRR通路中,体系变异频率最高的3个基因是CDK12(9.7%)、ATM(4.7%)、BRCA2(3.9%),胚系变异频率最高的3个基因则是BRCA2(3.1%)、PALB2(1.9%)、BRCA1(1.6%)。25.6%(64/250)的患者携带HRR基因变异。在HRD评分监测HRR变异呈阳性的患者中,仅有8.9%(4/45)例携带多个HRR基因变异,更多的病例携带单个HRR基因变异[CDK12占比40.0%(18/45),ATM/BRCA2占比17.8%(8/45),BRCA1占比11.1%(5/45),PALB2/FANCA占比2.2%(1/45)]。在这45例患者中共检测到61个HRR基因变异,其中HRR基因最常见变异类型为单碱基替换(47.5%,29/61)。CNV缺失的变异类型仅在体细胞样本中被检测到(14.8%,9/61)。HRR变异组的HRD评分的明显高于HRR野生组(中位HRD评分:突变组vs野生组:23.5vs19.0,P为0.0097)。但CNV缺失与其他变异类型之间的HRD评分没有显著性差异。此外,HRR变异组的TMB水平往往高于HRR野生组(中位TMB:突变组vs野生组:4.5vs2.8Muts/Mb,P=0.5)。
结论:研究揭示了中国前列腺癌人群HRR基因的分子特征,表明HRR基因变异(包括CNV缺失)与高HRD评分相关。这些数据为PARPi个体化治疗的临床管理提供了进一步的证据支持。
Abstract #5020;Poster #204
MAGNITUDE研究中使用尼拉帕利(NIRA)和阿比特龙加泼尼松(AAP)在转移性去势抵抗性前列腺癌(mCRPC)患者及同源重组修复(HRR)基因突变的逐基因分析
Author:Shahneen Sandhu MBBS, FRACP
背景:Ⅲ期临床研究MAGNTUDE发现,NIRA + AAP显著改善了mCRPC和HRR基因改变患者的治疗结果。很少有数据支持在BRCA1/2以外的HRR基因突变患者中使用PARP抑制剂。本次大会报道了关于NIRA+AAP对mCRPC患者以及除BRCA1/2外符合条件的单基因HRR突变患者的疗效。
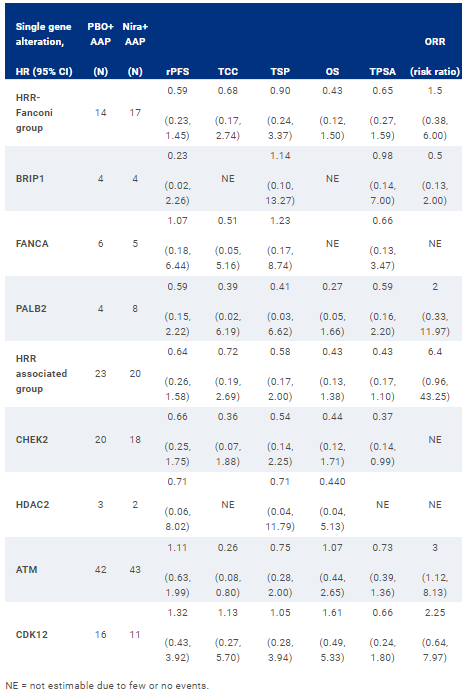
方法:对ATM、BRIP1、CDK12、CHEK2、FANCA、HDAC2或PALB2基因发生突变(不包括共突变)的186名患者(91例随机分为NIRA+AAP,95例随机分为PBO+AAP)的主要终点[BICR评估的影像学无进展生存期(rPFS)]、次要终点(至细胞毒性化疗时间[TCC],至症状进展时间[TSP],总生存期[OS])、PSA进展时间(TPSA)和客观缓解率(ORR)进行了预先指定的分析。这种对个体变化的分析并不能用于正式的统计推断。考虑到一些改变的罕见性,基于功能相似性的分组也被提出。
结果:PALB2或CHEK2突变的患者在所有终点均有改善。在ATM突变的患者中,观察到TCC、TSP、TPSA和ORR的获益。CDK12突变的患者只有TPSA和ORR有获益。当合并为功能组时,HRR -Fanconi通路发生突变的患者(BRIP1、FANCA、PALB2)与HRR相关突变的患者(CHEK2或HDAC2)所有终点均有改善。
结论:这些数据支持了MAGNITUDE初步分析的总体结论,并支持了NIRA+AAP在HRR突变除了BRCA1/2以外患者中的获益。
Abstract #5060;Poster #243
MAGNITUDE研究中使用尼拉帕利(NIRA)与阿比特龙加泼尼松(AAP)的转移性去势抵抗性前列腺癌(mCRPC)患者和同源重组修复(HRR)基因突变患者的健康相关生活质量(HRQoL)与疼痛情况
Author:Dana E. Rathkopf MD
背景:来自国际、随机、双盲、Ⅲ期临床研究MAGNITUDE研究显示,NIRA+AAP改善了影像学无进展生存期、至细胞毒性化疗时间和至症状进展时间,对mCRPC和HRR突变(9基因组检测)的患者毒性可控。本次大会报道了关于MAGNITUDE研究中的HRQoL与疼痛的数据。
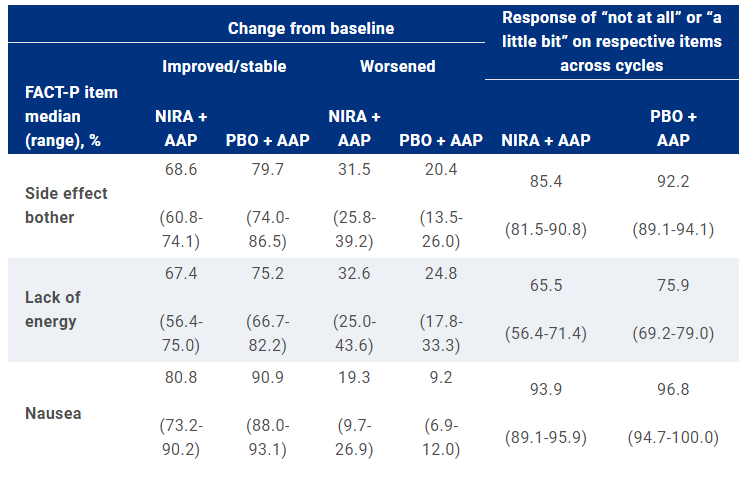
方法:符合条件的mCRPC和HRR突变患者按1∶1的比例随机分为NIRA+AAP组或安慰剂(PBO)+AAP组,周期28天。用药前筛选了ECOG状态≤1,简明疼痛评估量表( BPI-SF )最高疼痛评分≤3的患者。特定周期第1天的HRQoL评估包括前列腺癌治疗功能评估(FACT-P)和BPI-SF。使用重复测量分析比较各治疗组与基线的变化。采用比例风险回归模型比较两组间最严重疼痛强度的恶化时间(TTD)。
结果:FACT-P和BPI-SF的符合率均& 80%。大多数患者会随着时间的推移保持较低的疼痛水平。重复测量分析显示,随着时间的推移或两组之间的疼痛没有临床意义的差异。两组疼痛强度均未达到中位TTD。在第25百分位,NIRA+AAP与PBO+AAP相比,疼痛强度有延长的趋势(11.1个月vs10.1个月;HR,0.87;95%CI,0.61-1.24)。NIRA+AAP维持了HRQoL,而FACT-P总值随时间推移在两组间无临床意义差异。与PBO+AAP相比, NIRA+AAP 组FACT-P身体健康状况在早期有更大的恶化趋势,其原因是NIRA+AAP已知安全性范围内的事件(由于副作用导致的乏力和恶心);但总体而言,大多数患者报告的副作用影响很小。
结论:在MAGNITUDE研究中,大多数患者随着时间的推移保持了较低的疼痛水平和积极的HRQoL,不同治疗组之间没有临床意义上的差异,这更进一步支持对mCRPC和HRR突变的患者使用NIRA+AAP。两个治疗组的副作用影响都很低。尽管多数使用NIRA+AAP的患者报告了更严重的副作用,但其副作用表现出的症状被普遍认为是轻微的。
Abstract #5088;Poster #271
术前使用PSMA PET检测前列腺外病灶对根治性前列腺切除术患者无生化复发生存率的预测价值:多中心前瞻性 3 期影像学试验的随访分析。
Author:Loic Djaileb
背景:评估对接受根治性前列腺切除术 (RP) 和盆腔淋巴结清扫术 (PLND) 治疗的中高危前列腺癌患者使用FDA批准的68Ga-PSMA-11 PET进行分层,是否无生化复发生存期 (BCR-FS) 具有预测价值。
方法:这是一项对多中心、前瞻性3期影像学试验(n = 764;NCT03368547、NCT02611882、NCT02919111)的疗效分析队列的事后随访研究,评估了68Ga-PSMA-11 PET 对在中高危前列腺癌患者RP和PLND之前对转移灶的诊断准确性。每个PSMA-PET影响由三个独立审阅者阅读,读者分区域进行评估(阳性与阴性):前列腺床 (T)、盆腔淋巴结 (N)、盆腔外淋巴结 (M1a)、 骨 (M1b) 和内脏 (M1c),通过手术病理报告评估盆腔淋巴结转移的存在(pN0 vs pN1)。调查人员通过电子病历对患者RP后生化进展情况进行随访,BCR 定义为在RP后PSA& 0.2 ng/ml或进行补救治疗。使用对数秩检验进行成对比较,以评估术前 PSMA 扫描读数(N0M0 与 N+ 和/或 M+)和组织病理学状态(pN0 与 pN1)之间的 BCR-FS。
结果:2015年12月至2019年12月,共有764名患者入组该试验。277/764 (36%) 在 PSMA-PET后接受了RP,对 240/277 (87%) 名患者进行了临床随访,中位年龄为67岁 中位随访时间为21.4个月(IQR:8.80 - 31.53)。观察到 100 起 BCR 事件(41%),98/240 名患者接受了挽救治疗或其他治疗(40.6%)。整个队列的 BCR-FS 为 24.3 个月(IQR: 7.8 - 48.8)。pN0/PSMA-(N0 和 M0)、pN+/PSMA+(N+ 和/ 或 M+)、pN+/PSMA- 和 pN0/PSMA+的患者分别有160/240 (66%)、28/240 (11.6%)、39/240 (16%)、13/240 (5.4%) 。PSMA-患者的BCR-FS高于PSMA+ 患者(33个月vs7.3个月;p < 0.0001)。pN0/PSMA- 患者的 BCR-FS 高于 pN+/PSMA-、pN0/PSMA+ 和 pN+/PSMA+ 患者:46 个月 vs 12.3、11.7 和 3 个月(p < 0.001)。pN0/PSMA+ 和 pN+/PSMA- 之间的 BCR-FS 没有显着差异(11.7 对 12.3;p = 0.64)。
结论:PSMA PET分层可预测中高危前列腺癌患者RP后的BCR-FS。术前 PSMA-PET 扫描检测到前列腺外病灶的患者具有很高的生化复发风险。
Abstract #5005
SHR3680联合ADT对比比卡鲁胺+ADT治疗高瘤负荷mHSPC的3期临床研究
Author:Ding-Wei Ye
背景:TITAN 和 ARCHES 研究均表明,第二代雄激素受体抑制剂 (ARI) 联合ADT 与安慰剂联合ADT 相比,在 mHSPC的治疗中具有显着临床获益。然而,第一代ARI联合ADT广泛应用于临床,第二代ARI与第一代相比的优势有多大仍有待确定。这项研究评估了 SHR3680(一种新型口服二代ARI)对比比卡鲁胺在高瘤负荷mHSPC中的疗效和安全性。
方法:该研究是一项随机、开放标签、3 期研究 (NCT03520478),mHSPC 患者 以 1:1 的比例随机分配至SHR3680 (240 mg/d)联合ADT 或比卡鲁胺 (50 mg/d)联合ADT。按照CHARTED 研究定义的肿瘤负荷分层,所有患者都是高瘤负荷。主要终点是由独立审查委员会 (IRC) 评估的影像学无进展生存期 (rPFS) 和总生存期 (OS)。截至2021年5月16日,发生209例rPFS事件和153例死亡事件,进行了预先计划的rPFS中期分析。
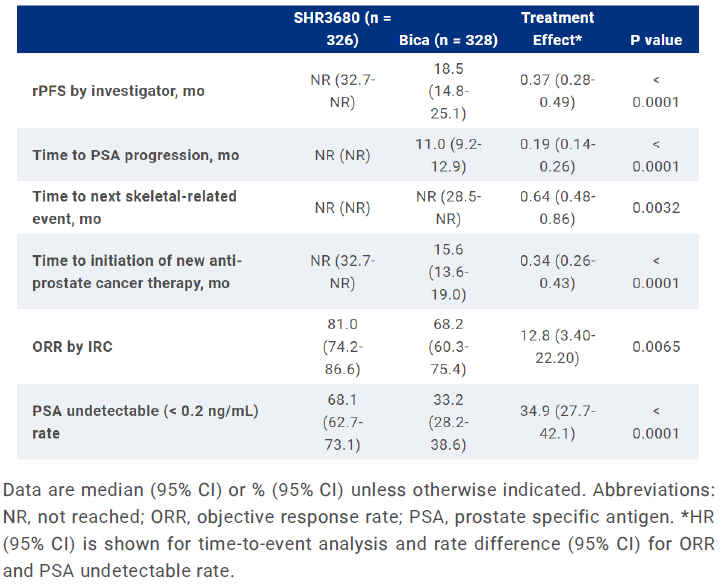
结果:654名患者被随机分配至SHR3680组 (n = 326)和B比卡鲁胺组 (n = 328),在数据截止时,SHR3680组的中位随访时间为22.1个月,比卡鲁胺组为20.4个月。与比卡鲁胺联合ADT相比,SHR3680联合ADT显着降低了放射学进展或死亡风险(HR,0.44;95% CI,0.33-0.58;p < 0.0001;中位值,未达到vs 25.1个月)。OS 数据不成熟,但与比卡鲁胺组相比,SHR3680组的OS有所改善(HR,0.58;95% CI,0.42-0.80;p = 0.0009)。所有次要疗效终点均支持 SHR3680联合ADT(见表格)。所有级别的任何原因导致的不良事件发生率两组是相似的,SHR3680组和比卡鲁胺组的≥3 级治疗相关不良事件分别是19.2% 和 13.9% ,SHR3680组无癫痫发生。
结论:与比卡鲁胺联合ADT相比,SHR3680 联合ADT显着改善了高瘤负荷mHSPC 的rPFS,安全性较为良好。
Abstract #5083;Poster #266
三联方案(NHT + DOC + ADT)与ADT联合新型内分泌治疗的双联方案在转移性去势抵抗性前列腺癌患者中疗效的间接比较。
Author:Syed Arsalan Ahmed Naqvi
背景:ARASENS和PEACE-1研究表明,在转移性去势抵抗性前列腺癌(mCSPC)患者中,雄激素剥夺疗法(ADT)和多西他赛(DOC)的基础上联合新型内分泌治疗(NHT)的三联方案对比DOC+ADT的双联方案,三联方案更有利于患者生存。然而,三联方案对比NHT+ADT的双联方案在生存获益方面的表现却缺乏探索。
方法:检索了MEDLINE、EMBASE和近期的会议论文集,纳入mCSPC患者接受三联方案的III期临床研究,以评估联合多西他赛和未联合多西他赛患者的治疗获益是否具有差异。结果包括总生存期(OS)和影像学无进展生存期(rPFS)。
结果:这项荟萃分析纳入5项临床研究(ARASENS、PEACE-1、ENZAMET、ARCHES和TITAN),共计5804例患者(联合多西他赛组:2836例;未联合多西他赛组:2836例)。亚组分析表明,三联方案(NHT + DOC + ADT; HR,0.74;95%CI 0.66-0.84;I2:0%)对比没有使用多西他赛的双联方案(NHT + ADT;HR,0.61;95%CI,0.53-0.70;I2 0%)具有显著的OS获益(交互检验p值:0.04),然而在rPFS方面没有观察到显著的统计学差异(p值:0.46)。全队列分析表明,三联方案(NHT + DOC + ADT)较双联方案(DOC + ADT)改善OS (HR,0.74;95%CI,0.66-0.84),但较NHT + ADT的双联方案相比则没有OS获益(HR,0.97;95%CI 0.78-1.20)。与DOC + ADT相比,NHT + ADT显著改善OS (HR 0.77;95%CI 0.64-0.92)。同样的,与DOC + ADT相比,NHT + DOC + ADT组rPFS明显改善(HR,0.49;95%CI,0.42-0.57),但与NHT + ADT相比则没有rPFS获益(HR,0.82;95%CI,0.65-1.04)。与DOC + ADT相比,NHT + ADT可改善rPFS(HR,0.60;95%CI 0.50-0.72)。
结论:这项探索性、假设性的分析表明,三联方案(NHT + DOC + ADT)方案较双联方案(ADT+NHT)可能不会延缓疾病进展或延长生存。这些发现为该领域未来的临床研究提供了方向,并表明了三联方案与双联方案(ADT+NHT)在临床应用时应如何平衡。因为该分析没有考虑潜在的混杂关系,如肿瘤负荷,所以该研究结果还需要谨慎解读。
Abstract #5076;Poster #259
一项随机II期试验LACOG 0415:研究雄激素信号通路抑制剂联合或不联合雄激素剥夺疗法(ADT)治疗去势敏感的前列腺癌的生存分析
Author:Fernando Cotait Maluf
背景:LACOG 0415 是一项 II 期开放标签临床试验,旨在评估晚期去势敏感型前列腺癌 (CSPC) ADT治疗的替代疗法。
方法:部晚期、高危生化复发或转移性 CSPC 患者被随机 (1:1:1) 分配接受 ADT 联合醋酸阿比特龙加泼尼松龙 (ADT+AAP)、单用阿帕鲁胺 (APA) 或阿帕鲁胺联合阿比特龙加泼尼松(APA+AAP)。该研究的主要终点是在治疗到25周时达到PSA≤0.2 ng / mL患者的比例。到第25周时,无疾病进展且有临床获益的患者可由医生自行决定维持治疗。此次,我们介绍了2年总生存期(2y-OS)和治疗失败时间(TTF)的结果。事件发生时间终点采用Kaplan-Meier曲线方法估计,并采用分层对数秩检验进行对比。
结果:128名患者被随机分配到ADT + AAP(n = 42),APA(n = 42)和APA + AAP(n = 44)组。治疗至25周时,ADT+AAP,APA和APA+AAP三组PSA≤0.2 ng/mL的患者比例分别为75.6% (95%CI 59.7%-87.6%),60.0% (95%CI 43.3%-75.1%)和79.5% (95%CI 63.5%-90.7%)。25周后还有110名患者继续治疗。2年访视时,80名(62.5%)患者仍在接受研究药物治疗。ADT+AAP组的中位治疗失败时间(TTF)为24个月(95%CI 23.3 - 24.0),APA组的中位治疗失败时间(TTF)为24个月(95%CI不可评估),APA+AAP组的中位治疗失败时间(TTF)为24个月(95%CI 13.0-24.0)。停止治疗的主要原因包括疾病进展(n = 8,6.3%),毒副反应(n = 10,7.8%),死亡(n = 6,4.7%),撤出(n = 4,3.1%)和其他(n = 19,14.8%)。预估2年存活患者的比例(2y-OS率)分别为:ADT+AAP组92.5% (95%CI 84.3-100),APA组 87.9% (95%CI 77.9-97.8),APA+AAP组92.7% (95%CI 84.8-100) (p = 0.5926)。第25周PSA ≤ 0.2 ng/mL患者的2y-OS 率为92.9% (95% CI 85.3 - 96.2),PSA & 0.2 ng/mL患者2y-OS 率为85.0% (95% CI 72.9-97.1) (p = 0.1250)。
结论:晚期激素敏感性前列腺癌患者使用ADT+阿比特龙,阿帕鲁胺,或者阿帕鲁胺+阿比特龙进行治疗均能取得高PSA反应率和比较好的2年OS率。治疗25周时 PSA ≤ 0.2 ng/mL似乎是晚期CSPC患者OS的替代预后预测因子。在总体入组人群中,第25周PSA≤0.2 ng/mL的患者比第25周PSA&0.2ng/mL的患者具有更高的2年OS率(92.9%对85.0%),然而没有显著性统计学差异。该临床试验编号为NCT02867020。
Abstract #5000
TheraP:177Lu-PSMA-617 (LuPSMA) 与卡巴他赛在经多西他赛治疗进展的转移性去势抵抗性前列腺癌 (mCRPC) 患者中的疗效比较 —— 中位随访 3 年后的总生存期分析(ANZUP 1603)
Author:Michael S Hofman
背景:此前曾报道(Lancet 2021),将经多西他赛进展后的mCRPC患者随机分为LuPSMA组与卡巴他赛组,LuPSMA组显著提高了PSA反应率(66% vs. 37%),RECIST 客观反应率 (49% vs. 24%),PFS (HR 0.63),并且3-4级不良反应更低(33% vs. 53%),患者主述也更好。此次报道了次要终点OS,包括试验参与者以及最初由于PSMA低表达或者PSMA-PET与 FDG-PET结果不一致而被排除的患者。
方法:TheraP试验入组要求多西他赛进展的mCRPC患者,68Ga-PSMA-11 PET显示高PSMA表达(至少一个部位具有SUVmax≥20),并且没有18F-FDG显示阳性而PSMA是阴性结果(不一致疾病)。患者被随机分配为LuPSMA(每6周8.5-6GBq,最多6个周期)与卡巴他赛(每3周20mg / m2,最多10个周期)治疗。OS通过意向性分析处理,考虑到非等比例的风险,用限制平均生存时间(RMST)进行总结。
结果:2018年2月6日至2019年9月3日期间对291例患者进行了筛查:200例符合入组条件,随机分配为LuPSMA组(99例)或卡巴他赛组(101例);最初符合要求的291例患者中,有80例患者由于PSMA/FDG-PET(51 SUVmax < 20, 29 不一致)检查不合格而被排除,这80例患者中有61例(76%)进行了随访。中位随访36个月后(数据截止时间为2021年12月31日),卡巴他赛报道死亡例数70/101,LuPSMA组死亡例数为77/99,PSMA/FDG-PET排除的可随访61名患者中死亡例数为55/61。进展后的后续治疗情况,卡巴他赛组有21例仍然接受卡巴他赛治疗,20例换成了LuPSMA;LuPSMA组有5例仍然接受LuPSMA治疗,32例换成卡巴他赛治疗。LuPSMA组与卡巴他赛组的OS相似(36个月的RMST为19.1 vs.19.6个月,差异为-0.5,95%CI -3.7至+ 2.7)。更长的随访时间并没有发现额外的安全性信号。61例由于PSMA/FDG-PET检查而在随机化之前被排除的患者中36个月的RMST为11.0个月(95%CI 9.0-13.1),其中29例(48%)接受了卡巴他赛治疗,3例(5%)接受了LuPSMA治疗。
结论:LuPSMA是多西他赛进展的mCRPC患者的可选方案,有着更低的不良事件发生率,更高的反应率,患者主述也更好,与卡巴他赛有相似的OS。由于PSMA 低表达或者FDG-显示不一致疾病而被排除的患者中位生存期更短,否则这些患者也可以接受LuPSMA治疗。临床试验编号:NCT03392428。
审批号:CN-99133 Expiration Date:2022-9-8
本文的采访/撰稿/发布由阿斯利康提供支持,仅供医疗卫生专业人士参考
参考资料:
[1].https://meetings.asco.org/abstracts-presentations/212388
[2].https://meetings.asco.org/abstracts-presentations/212541
[3].https://meetings.asco.org/abstracts-presentations/211031
[4].https://meetings.asco.org/abstracts-presentations/211543
[5].https://meetings.asco.org/abstracts-presentations/212246
[6].https://meetings.asco.org/abstracts-presentations/208941
[7].https://meetings.asco.org/abstracts-presentations/211665
[6].https://meetings.asco.org/abstracts-presentations/212246
[7].https://meetings.asco.org/abstracts-presentations/212195
[8].https://meetings.asco.org/abstracts-presentations/207021
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |