*仅供医学专业人士阅读参考
王常玉教授详解替雷利珠单抗新适应证获批背景及其意义!
宫颈癌、子宫内膜癌、卵巢癌是严重威胁女性生命健康的三大妇科恶性肿瘤。近年来,免疫治疗的问世改善了多个瘤种患者的生存以及生活质量,其中也包括妇瘤患者。目前,在妇科恶性肿瘤中,免疫治疗已经在美国国家综合癌症网络(NCCN)子宫内膜癌和宫颈癌指南中得到了推荐[1-2]。
2022年3月11日,百济神州PD-1抑制剂替雷利珠单抗正式获得中国药品监督管理局(NMPA)批准,用于治疗既往经治、局部晚期不可切除MSI-H/dMMR实体瘤患者。本次获批对妇瘤诊疗领域有怎样的意义?“医学界肿瘤频道”特邀华中科技大学同济医学院附属同济医院王常玉教授就妇科肿瘤的诊疗现状及免疫治疗的应用现状进行分享。
免疫治疗妇瘤值得期待,有望成为妇瘤治疗新“主力军”
王常玉教授介绍道:“子宫内膜癌、宫颈癌、卵巢癌是严重威胁妇女健康的三大恶性肿瘤。传统的治疗手段有手术、化疗和放疗。近年来靶向治疗和免疫治疗的飞速发展,在妇科恶性肿瘤领域也取得了一些突破。如PARP抑制剂在晚期卵巢癌维持治疗中的应用,明显改善了晚期上皮性卵巢癌的预后。抗血管生成药物在晚期卵巢癌、晚期复发内膜癌、子宫颈癌方面的应用也使患者的生存有改善。随着免疫检查点抑制剂在肿瘤治疗领域研究不断深入,在妇科恶性肿瘤的临床应用研究也越来越多,也取得了很大的进展。
子宫内膜癌的免疫治疗
近年研究发现,子宫内膜癌中PD-(L)1的表达比例较高,其中的子宫内膜样癌PD-(L)1的表达比例高达40%~80%,透明细胞癌约为23%~69%,浆液性癌约为10%~68%,同时子宫内膜癌中MSI-H/dMMR的发生率为37%~40%,因此子宫内膜癌属于在免疫检查点抑制剂(ICI)中获益较高的妇科恶性肿瘤[3]。
免疫单药方面,KEYNOTE系列研究显示,帕博利珠单抗治疗至少接受一次标准化疗后进展的晚期或复发子宫内膜癌患者,其中MSI-H/dMMR 患者的客观缓解率(ORR)为53%~57%, TMB-H患者为46.7%,PD-L1阳性患者为13%。此外,GARNET研究评估了dostarlimab-gxly用于含铂治疗后进展或MSI-H/dMMR子宫内膜癌患者的疗效,结果显示ORR为44.7%,疾病控制率(DCR)为57.3%。这些研究均支持PD-L1单抗用于经治的MSI-H/dMMR晚期、复发子宫内膜癌的治疗[4-6]。
免疫联合治疗方面,KEYNOTE-146评估了帕博利珠单抗联合仑伐替尼用于既往接受不超过二线化疗且有可测量病灶的晚期子宫内膜癌患者的疗效和安全性,结果显示,非pMMR患者的ORR为37.2%,MSI-H/dMMR患者为63.6%,中位缓解持续时间(DOR)为21.2个月,中位PFS为7.4月,中位OS为16.7个月,联合方案不仅在MSI-H患者中疗效显著,而且在MSS患者中也优于单药治疗;KEYNOT-775 III期研究同样显示,帕博利珠单抗联合仑伐替尼治疗既往至少接受一线含铂化疗的晚期复发子宫内膜癌患者,使其中pMMR患者相比化疗延长了2.8个月PFS和5.4个月中位OS,ORR提高15.2%,对于总体人群,中位PFS延长3.4个月,复发和死亡风险降低44%,中位OS延长6.9个月,ORR提高17.2%。指南基于此推荐帕博利珠单抗联合仑伐替尼用于MSI-H/dMMR 晚期复发子宫内膜癌患者[7-8]。
宫颈癌的免疫治疗
早期宫颈癌患者通过手术及放疗、化疗可以取得较好的预后。然而晚期复发宫颈癌的治疗始终是治疗难点,疗效亟待改善。宫颈癌患者中MSI-H/dMMR患者的比例较低,仅为2.26%左右,但宫颈癌患者PD-L1阳性患者的比例高达34.4%,甚至有文献报道高达96%,这提示PD-1抑制剂有望用于晚期宫颈癌的治疗。目前免疫治疗在宫颈癌领域已经取得了一定进展,免疫治疗联合化疗、放疗、PARP抑制剂、TKI药物等治疗宫颈癌的临床试验均在进行中,并且部分研究已经取得了可观的疗效。
就免疫单药治疗而言,在KEYNOTE系列研究显示,帕博利珠单抗治疗PD-L1阳性患者的ORR为14.6%~17.0%。另有数项研究结果表明,纳武利尤单抗单抗治疗晚期/复发子宫颈癌的ORR为4.0%~26.3%。KEYNOTE-158和JapicCTI-163、212研究均根据患者PD-L1表达状况进行了亚组分析,结果显示PD-L1阳性者对PD-1抑制剂的反应性较好。此外,EMPOWER/GOG-3016/ENGOT-cx9 III期研究表明,与单药化疗相比,西米普利单抗可显著改善既往经一线含铂化疗进展后的晚期转移性子宫颈癌患者的OS,且与PD-L1表达状况和组织学类型无关,西米普利单抗降低了25%的复发/死亡风险。
就免疫联合治疗而言,KEYNOTE-826 Ⅲ期研究探索了帕博利珠单抗+含铂化疗±贝伐珠单抗一线治疗复发转移子颈癌患者的疗效与安全性。研究结果显示,与对照组相比,无论PD-L1表达状态如何,联合治疗均能显著提高PFS(10.4月vs 8.2月,HR=0.65)和OS(24.4月vs 16.5月,HR=0.67)[6],2022年NCCN子宫颈癌指南已基于此推荐帕博利珠单抗联合化疗一线治疗晚期复发、转移性宫颈癌,奠定了免疫治疗在宫颈癌中的一线治疗地位[1]。
卵巢癌的免疫治疗
就卵巢癌而言,多数卵巢癌为浆液性上皮性卵巢癌,MSI-H患者比例低,据报道称仅占1.37%,TMB-H患者也仅占1.47%,PD-L1阳性表达者大约10%~30%。因此,免疫检查点抑制剂在卵巢癌中的疗效有限。
在免疫单药方面,NINJA和JAVELIN Ovarian 200两项研究提示,免疫检查点抑制剂单药治疗相比化疗并未改善卵巢癌患者的预后,总体反应率不高。目前,基于帕博利珠单抗已获批dMMR/MSI-H和TMB-H实体瘤患者的适应证,临床上仅推荐帕博利珠单抗用于治疗伴有dMMR/MSI-H或TMB-H复发卵巢癌患者的治疗。
在免疫联合治疗方面,就联合化疗而言,JAVELIN Ovarian 100研究探究了紫杉醇+卡铂化疗联合avelumab治疗初治卵巢癌患者并使用avelumab维持治疗的疗效,结果表明免疫联合治疗及维持治疗相比化疗并未展现PFS获益,该研究也因故提前中止。对于铂耐药复发卵巢癌,部分免疫联合化疗的研究显示了ORR的一定提高,但反应时间较短。基于此,目前尚不推荐免疫检查点抑制剂联合化疗。就联合靶向药物而言,目前仅有Ⅰ、Ⅱ期的研究结果,总体ORR为15%~32%。就联合PARP抑制剂而言,MEDIOLA研究显示,奥拉帕利+度伐利尤单抗治疗gBRCA突变、铂敏感复发卵巢癌患者的ORR达71.9%,但TOPACIO/KEYNOTE-162研究中尼拉帕利联合帕博利珠单抗治疗铂耐药卵巢癌患者的ORR仅为18%。基于以上研究,免疫检查点抑制剂联合某些靶向药物虽然显示出一定疗效,但尚待更多研究证据,暂不足以推荐临床应用。
王常玉教授谈道:“总体而言,免疫治疗对部分妇科恶性肿瘤已经显示出一定临床疗效,目前在三大妇科恶性肿瘤中,免疫治疗在子宫内膜癌中疗效最好,其次是宫颈癌,而卵巢癌疗效最差。此外,在适用ICI治疗前筛选治疗优势人群至关重要,同时ICI与化疗、抗血管生成治疗、PARP抑制剂等联合有望提高疗效。”
研究符合国情,药品结构创新,替雷利珠单抗为妇瘤患者带来切实获益
王常玉教授表示:“值得注意的是,虽然以免疫治疗为基础的治疗方案已经在妇科肿瘤领域展现了可观疗效,但既往的相关研究中缺乏针对中国患者的数据,因此对我国临床实践的指导作用可能相对有限。
RATIONALE-209研究是首个国产PD-1单抗治疗我国MSI-H/dMMR妇科肿瘤患者的研究,评估了替雷利珠单抗单药治疗经治、局部晚期不可切除或转移性MSI-H/dMMR实体瘤患者有效性和安全性,其最新结果于2022 美国妇科肿瘤协会(SGO)大会上公布。
RATIONALE-209研究纳入了80例局部晚期不可切除或者转移性MSI-H/dMMR实体瘤患者,其中17例为妇瘤患者(15例子宫内膜癌,1例宫颈癌,1例卵巢癌)。研究结果显示,在可评估的所有妇科肿瘤患者中,客观缓解率(ORR)为53.3%,完全缓解(CR)率为20%,疾病控制率(DCR)为60.0%。其中,子宫内膜癌患者ORR为46.2%,CR率为23.1%,DCR为53.8%;且宫颈癌与卵巢癌患者也均获得部分缓解(PR)的疗效[7]。
表1. RATIONALE-209研究疗效数据
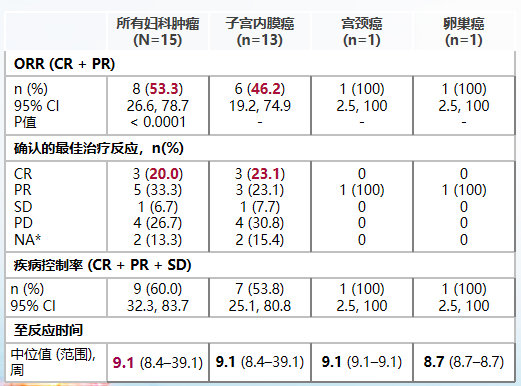
此外,替雷利珠单抗治疗的中位至缓解时间(TTR)为9.1周,治疗起效较快。截至中位随访时间17.5个月时,妇瘤队列的中位缓解持续时间(DoR)、PFS和OS均未达到。安全性方面,患者整体耐受性良好、不良反应可控,未发现新的安全性信号[9]。
谈及替雷利珠单抗的独特之处,王常玉教授介绍道:“替雷利珠单抗独特的药物结构设计使其具有更长的半衰期,能够在体循环中维持更长的时间,因此有着更强的抗肿瘤活性。此外,传统PD-1单抗的Fc段可通过结合巨噬细胞和NK细胞引起抗体依赖细胞吞噬作用(ADCP)和抗体依赖细胞毒作用(ADCC),从而导致T细胞损耗,而替雷利珠单抗抗体部分的Fc段进行了改造,最大程度地消除了替雷利珠单抗的ADCP效应,避免了T细胞损耗对抗肿瘤治疗疗效的影响。同时,其抗体Fab段与PD-1结合位点面大,与PD-1的亲和力更高,可更彻底地阻断PD-1与PD-L1结合。
王常玉教授总结道:“由于替雷利珠单抗的RATIONALE-209研究是针对我国患者的研究,更符合我国的临床实践,因此有着很强的指导意义。也正是基于这项研究,替雷利珠单抗在我国获批用于治疗既往经治、局部晚期不可切除MSI-H/dMMR实体瘤患者,得以进一步造福我国患者。”
专家简介

王常玉 教授
三级教授,主任医师,博士生导师
华中科技大学同济医学院附属同济医院
妇科肿瘤专科党支部书记兼副主任
中国老年医学会妇科分会常委
湖北省医学会妇科肿瘤分会委员
武汉市医学会妇产科分会委员
肿瘤防治研究杂志常务编委
湖北省妇科肿瘤质控专家委员会副主委
湖北省干部医疗保健专家
主持和参与多项国家自然科学基金课题,发表SCI论文30余篇,参编现代妇产科学、临床妇产科学、妇科肿瘤诊治经验荟萃等多部专著,作为主要参与者参加的卵巢癌进展机制及其阻碍策略的研究与应用获国家科学技术进步二等奖。连续多年手术量在全院居前十
参考文献
[1].National Comprehensive Cancer Network.NCCN Clinical Practice Guidelines in Oncology-Uterine Neoplasms.Version 1.2022.
[2].National Comprehensive Cancer Network.NCCN Clinical Practice Guidelines in Oncology-Cervical Cancer.Version 1.2022.
[3].Liu J, Wang Y, Tian Z, et al. Multicenter phase II trial of Camrelizumab combined with Apatinib and Eribulin in heavily pretreated patients with advanced triple-negative breast cancer. Nat Commun. 2022 May 31;13(1):3011.
[4].Le DT, Uram JN, Wang H, et al. PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N Engl J Med. 2015. 372(26): 2509-20.
[5].O'Malley DM, Bariani GM, Cassier PA, et al. Pembrolizumab in Patients With Microsatellite Instability-High Advanced Endometrial Cancer: Results From the KEYNOTE-158 Study. J Clin Oncol. 2022 Jan 6:JCO2101874.
[6].Ott PA, Elez E, Hiret S, Kim DW, Morosky A, Saraf S, Piperdi B, Mehnert JM. Pembrolizumab in Patients With Extensive-Stage Small-Cell Lung Cancer: Results From the Phase Ib KEYNOTE-028 Study. J Clin Oncol. 2017 Dec 1;35(34):3823-3829.
[7].Makker V, Colombo N, Casado Herráez A, et al. Lenvatinib plus Pembrolizumab for Advanced Endometrial Cancer. N Engl J Med. 2022 Feb 3;386(5):437-448.
[8].Matthew H. Taylor et al. Phase IB/II Trial of Lenvatinib Plus Pembrolizumab in Patients With Advanced Renal Cell Carcinoma, Endometrial Cancer, and Other Selected Advanced Solid Tumors. J Clin Oncol 2020.
[9].Dong Wang, et al. 2022 SGO. Abstract #127.
*此文仅用于向医学人士提供科学信息,不代表本平台观点


| 留言与评论(共有 0 条评论) “” |